题目内容
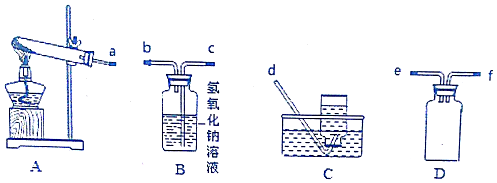
18.汽车尾气污染是造成雾霾天气的重要原因之一,解决这个问题除了限制汽车出行外,更重要的是研发催化汽车尾气的转化技术,该技术中催化剂及载体的选择和改良是关键,某稀土催化剂催化转化汽车尾气示意图如图甲
(1)下列有关说法正确的是bd.
a.C3H8与CH3CH=CH3一样,分子中碳原子都采用的是SP3杂化
b.N2、CO2、H2O都是非极性分子
c.每个CO2分子中,含有2个π键和2个σ键+
d.CO的一种等电子体为NO+,它的电子式为
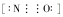
(2)CO与Fe可生成羰基铁[Fe(CO)5],已知其中铁为0价,铁原子的基态核外电子排布式为[Ar]3d64s2或者1s22s22p63s23p63d64s2,[Fe(CO)5],中配位原子是C,理由是配体中C的电负性小于O,C原子核提供孤店子对配位能力强于O原子.
(3)C、N、O三种元素的第一电离能由大到小的顺序是N>O>C,Al2O3晶体熔点高是耐火材料,AlCl3晶体易升华,熔点低,工业上电冶制取铝用前者而不用后者的原因是AlCl3晶体易升华,熔点低,是分子晶体,熔融时不导电,无法电解.
(4)钙钛矿型符合氧化物也可作为汽车尾气转化的催化剂,一种复合氧化物晶胞结构如图乙所示,则与每个Sr2+与12个O2-紧邻,若Sr2+与紧邻O2-的核间距为apm,阿伏加德罗常数为NA,则该氧化物晶体密度的计算表达式为$\frac{184}{NA(\sqrt{2}a×1{0}^{-10})^{3}}g/c{m}^{3}$.
分析 (1)a.C3H8分子中,C原子采用sp3杂化;但是CH3CH=CH3,C原子采用sp3、sp2杂化;
b.同种元素之间形成非极性共价键,不同元素之间形成极性共价键,分子中正负电荷中心不重合,从整个分子来看,电荷的分布是不均匀的,不对称的,这样的分子为极性分子,以极性键结合的双原子一定为极性分子,以极性键结合的多原子分子如结构对称,正负电荷的重心重合,电荷分布均匀,则为非极性分子;
c.根据单键为σ键,双键含有1个σ键和1个π键,三键含有1个σ键和2个π键分析;
d.根据等电子体的定义,只要原子数目和电子总数(或价电子总数)相同就是等电子体,等电子体结构相似;
(2)Fe的原子序数为26,根据能量最低原理和洪特规则书写电子排布式;配位体:提供孤电子对的分子或离子;配位原子:配体中,提供电子对的原子;
(3)根据第一电离能的定义判断,指基态的气体原子失去一个电子形成+1价气态阳离子时所需的能量;根据物质性质及晶体类型选择冶制金属的方法;
(4)Sr2+在晶胞的体心,与之紧邻的O2-在晶胞的棱上;根据公式D=$\frac{MZ}{NAV}$计算晶体密度,据此分析解答.
解答 解:(1)a.C3H8分子中每个C含有4个σ键,且每个C原子价层电子对个数是4,则C原子采用sp3杂化;CH3CH=CH3分子中存在C-C单和C=C原子,且每个C原子价层电子对个数是4,则C原子采用sp3和sp2杂化,故a错误;
b.N2是以非极性键结合的双原子一定为非极性分子,CO2中含有极性键,为直线形分子,结构对称,分子中正负电荷重心重叠,为非极性分子,H2O的立体构型为v型,结构对称,分子重心重叠,为非极性分子,故b正确;
c.CO2的结构式为O=C=O,中含有2个π键,2个σ键,故c错误;
d.CO的一种等电子体为NO+,CO的结构为C≡O,则NO+的电子式为 ,故d正确;
,故d正确;
故答案为:bd;
(2)Fe的原子序数为26,根据能量最低原理和洪特规则可写出基态Fe原子核外电子排布式为1s22s22p63s23p63d64s2或者[Ar]3d64s2,[Fe(CO)5]中心原子是Fe,CO提供孤电子对为配体,配位原子是为C,理由是配体中C的电负性小于O,C原子核提供孤店子对配位能力强于O原子,
故答案为:1s22s22p63s23p63d84s2或者[Ar]3d64s2;C;配体中C的电负性小于O,C原子核提供孤店子对配位能力强于O原子;
(3)根据第一电离能的定义判断,指基态的气体原子失去一个电子形成+1价气态阳离子时所需的能量,即N>O>C;根据物质性质及晶体类型选择冶制金属的方法,因为AlCl3晶体易升华,熔点低,是分子晶体,熔融时不导电,无法电解所以电解Al2O3来制备金属铝,
故答案为:N>O>C;AlCl3晶体易升华,熔点低,是分子晶体,熔融时不导电,无法电解;
(4)Sr2+在晶胞的体心,与之紧邻的O2-在晶胞的棱上,12条棱,每个Sr2+紧邻的O2-有12;由晶胞结构得N(sr2+)=1,N(O2-)=12×$\frac{1}{4}$=3,N(Ti4+)=8×$\frac{1}{8}$=1 所以晶胞的分子式为SrO•TiO2则M=88+16+48+16×2=184g/mol,Z=1,∵Sr2+与紧邻O2-的核间距为apm,设晶胞的变成为x,则(2a)2=x2+x2解得x=$\sqrt{2}$a∴V=($\sqrt{2}$a×10-10)cm3 根据公式D=$\frac{MZ}{{N}_{A}V}$=$\frac{184}{{N}_{A}(\sqrt{2}a×1{0}^{-10})^{3}}g/c{m}^{3}$,
故答案为:12;$\frac{184}{{N}_{A}(\sqrt{2}a×1{0}^{-10})^{3}}g/c{m}^{3}$.
点评 本题是对物质结构的考查,涉及杂化、分子极性、等电子体、电子式、核外电子排布、配合物、晶体结构等,掌握相关知识是解答关键,题目难度中等.

 春雨教育同步作文系列答案
春雨教育同步作文系列答案| A. | 氢气 | B. | 石油 | C. | 沼气 | D. | 酒精 |
| A. | 鸡蛋清溶液中加入饱和(NH4)2SO4溶液生成白色沉淀,属于物理变化 | |
| B. | 将一束强光通过淀粉溶液,也能产生丁达尔效应 | |
| C. | 水泥厂、冶金厂常用高压电除去烟尘,是因为烟尘粒子带电荷 | |
| D. | 纳米材料粒子直径一般从几纳米到几十纳米(1 nm=10-9 m),因此纳米材料属于胶体 |
| A. | 氮气分子中含有1个σ键和2个π键 | |
| B. | 乙烯中C=C的键能是乙烷中C-C的键能的2倍 | |
| C. | N-O键的极性比C-O键的极性大 | |
| D. | NH4+中4个N-H键的键能不相同 |
 的命名正确的是( )
的命名正确的是( )| A. | 3-甲基-3-丁烯 | B. | 3-甲基-2-丁烯 | C. | 2-甲基-2-丁烯 | D. | 2-甲基-2-戊烯 |
| A. | 淀粉、油脂、蛋白质都属于高分子化合物 | |
| B. | 乙醇、乙酸、乙酸乙酯都能发生取代反应 | |
| C. | 聚乙烯、苯乙烯都能使溴的四氯化碳溶液和酸性KMnO4溶液褪色 | |
| D. | 硝基苯分子中苯环上的一个H被-C4H9取代后形成的有机物共有9种 |
| A. | 醇的官能团委羟基(-OH),它与氢氧根(OH-)具有相同的结构 | |
| B. | 工业酒精中往往含有甲醇,因此不可用来勾兑白酒 | |
| C. | 乙醇能够以任意比溶解于水,所以酒厂可以勾兑各种浓度的酒 | |
| D. | 乙醇,乙二醇,丙三醇分别属于一元醇、二元醇、三元醇 |
| 选项 | 实验目的 | 玻璃仪器 |
| A | 将溴水滴入KI溶液中,从溶液中分离生成的I2 | 胶头滴管、试管、漏斗、玻璃棒、烧杯 |
| B | 实验室通过蒸馏的方法除去自来水中含有的Cl-等杂质制取蒸馏水 | 酒精灯、圆底烧瓶、冷凝管、尾接管、锥形瓶 |
| C | 用植物油提取溴水中的Br2 | 铁架台、分液漏斗、玻璃棒、烧杯 |
| D | 用浓氨水和氢氧化钠固体制取氨气 | 酒精灯、烧杯、导管、集气瓶 |
| A. | A | B. | B | C. | C | D. | D |