题目内容
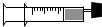
 实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )| 选项 | a中物质 | b中物质 | c中收集气体 | d中物质 |
| A | 浓氨水 | CaO | NH3 | H2O |
| B | 浓硫酸 | 浓盐酸 | HCl | NaOH溶液 |
| C | 稀硝酸 | Cu | NO2 | H2O |
| D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
| A、A | B、B | C、C | D、D |
考点:气体发生装置,气体的收集,尾气处理装置
专题:
分析:A、氨气密度小于空气的密度,收集方法应该为向下排空气法;
B、浓硫酸吸水、放热,浓盐酸挥发出HCl,HCl可采用向上排空气法,多余的HCl用NaOH溶液吸收;
C、稀硝酸与铜反应生成的是一氧化氮气体,d中用水无法吸收含一氧化氮或二氧化氮的尾气;
D、用MnO2和浓盐酸制取氯气时需要加热.
B、浓硫酸吸水、放热,浓盐酸挥发出HCl,HCl可采用向上排空气法,多余的HCl用NaOH溶液吸收;
C、稀硝酸与铜反应生成的是一氧化氮气体,d中用水无法吸收含一氧化氮或二氧化氮的尾气;
D、用MnO2和浓盐酸制取氯气时需要加热.
解答:
解:A、氨气的密度比空气密度小,应该采用向下排空气法收集,装置c中的导管应改为短进长出,故A错误;
B、浓硫酸吸水、放热,浓盐酸挥发出HCl,HCl可采用向上排空气法,多余的HCl用NaOH溶液吸收,故B正确;
C、铜与稀硝酸反应生成产物为一氧化氮,无法达到二氧化氮,一氧化氮、二氧化氮的尾气吸收不能使用水,故C错误;
D、用MnO2和浓盐酸制取氯气时需要加热,氯气的密度比空气大,能使用向上排空气法,氯气用氢氧化钠溶液吸收,故D错误;
故选B.
B、浓硫酸吸水、放热,浓盐酸挥发出HCl,HCl可采用向上排空气法,多余的HCl用NaOH溶液吸收,故B正确;
C、铜与稀硝酸反应生成产物为一氧化氮,无法达到二氧化氮,一氧化氮、二氧化氮的尾气吸收不能使用水,故C错误;
D、用MnO2和浓盐酸制取氯气时需要加热,氯气的密度比空气大,能使用向上排空气法,氯气用氢氧化钠溶液吸收,故D错误;
故选B.
点评:本题考查化学实验基本原理(气体的制备)、实验装置、仪器的使用,题目难度中等,注意掌握常见气体的制取原理、收集方法及尾气吸收方法,该考点是高考的热点,本题对相关的知识考查的要求较高,本题有利于培养学生对实验的分析能力.

练习册系列答案
 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
下列实验事实不能证明醋酸是弱酸的是( )
| A、常温下,等浓度的醋酸比盐酸导电能力弱 |
| B、常温下,测得0.1 mol?L-1醋酸溶液的pH=4 |
| C、常温下,将pH=1的醋酸溶液稀释1000倍,测得pH<4 |
| D、常温下,将物质的量浓度相同的醋酸溶液与氢氧化钠溶液等体积混合后恰好中和 |
对于平衡体系:aA(g)+bB(g)?Cc(g)+Dd(s)△H<0,下列判断中正确的是( )
| A、若a+b<c+d,则反应一定能自发向右进行 |
| B、若从正反应开始,起始时A、B的物质的量之比为a:b,则平衡时A、B的转化率之比也为a:b |
| C、若a+b=c+d,在平衡体系中共有气体m mol,再向其中充入n mol B,则达到平衡时气体总物质的量小于(m+n)mol |
| D、若a+b=c+d,则对于体积不变的容器,升高温度,平衡向左移动,容器中气体的压强一定不变 |
淀粉溶液是一种胶体,并且淀粉遇到碘单质可以出现明显的蓝色特征,现将淀粉和稀Na2SO4溶液混合,装在半透膜中,浸泡在盛有蒸馏水的烧杯中,过一段时间后,取烧杯中液体进行实验,能证明半透膜完好无损的是( )
| A、加入Ba(NO3)2溶液产生白色的沉淀. |
| B、加入碘水变蓝 |
| C、加入Ba(NO3)2溶液没有白色沉淀 |
| D、加入碘水不变蓝 |
下列操作中不正确的是( )
| A、过滤时玻璃棒与三层滤纸的一边接触 |
| B、蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶支管口处,且冷凝水方向应当由下往上 |
| C、加热试管内液体时 试管底部与酒精灯外焰接触 |
| D、向试管内滴加液体时胶头滴管紧贴试管内壁 |
最后,科学家研制出一种纸质电池,这种“软电池”采用薄层纸片作为载体和传导体,纸片一边附着锌,另一边附着二氧化锰.电池总反应为:Zn+2MnO2+H2O=ZnO+2MnO(OH).下列说法不正确的是( )
| A、该电池Zn为负极,MnO2为正极 |
| B、该电池的正极反应为:MnO2+e-+H2O=MnO(OH)+OH- |
| C、电池工作时水分子和OH-都能通过薄层纸片 |
| D、导电时外电路电子由Zn流向MnO2,内电路电子由MnO2流向Zn |
 某无色溶液中只可能含有NH4+、K+、Al3+、Mg2+、Fe3+、Cl-、CO32-、SO42-等离子中的几种离子.下列说法正确的是( )
某无色溶液中只可能含有NH4+、K+、Al3+、Mg2+、Fe3+、Cl-、CO32-、SO42-等离子中的几种离子.下列说法正确的是( )①取10mL该溶液于试管中滴加Ba(NO3)2溶液并加稀硝酸酸化后过滤得到0.03mol白色沉淀,向滤液中加入AgNO3溶液未见沉淀产生.
②另取10mL该溶液于试管中,滴加NaOH溶液产生白色沉淀,沉淀的量与所加氢氧化钠溶液体积如图所示.
| A、溶液中一定存在的离子有K+、NH4+、Al3+、SO42- |
| B、溶液中一定不存在的离子有Cl-、Fe3+、Mg2+、K+、CO32- |
| C、实验中NaOH溶液的物质的量浓度为0.lmol/L |
| D、实验中无法确定K+的存在 |