题目内容
12.在标准状况下,由CO和CO2组成的混合气体6.72L,质量为12g.此混合气体中CO和CO2物质的量之比为1:3,混合气体的平均相对分子质量是40,摩尔质量之比是7:11.分析 气体的物质的量为$\frac{6.72L}{22.4L/mol}$=0.3mol,设CO和CO2物质的量分别为x、y,则
$\left\{\begin{array}{l}{x+y=0.3}\\{28x+44y=12}\end{array}\right.$,
解得x=0.075mol,y=0.225mol,以此来解答.
解答 解:气体的物质的量为$\frac{6.72L}{22.4L/mol}$=0.3mol,设CO和CO2物质的量分别为x、y,则
$\left\{\begin{array}{l}{x+y=0.3}\\{28x+44y=12}\end{array}\right.$,
解得x=0.075mol,y=0.225mol,
此混合气体中CO和CO2物质的量之比为0.075mol:0.225mol=1:3,混合气体的平均相对分子质量是$\frac{12}{0.3}$=40,摩尔质量之比是28g/mol:44g/mol=7:11,
故答案为:1:3;40;7:11.
点评 本题考查物质的量的计算,为高频考点,把握质量、物质的量的关系为解答的关键,侧重分析与计算能力的考查,注意摩尔质量与相对分子质量的数值相同,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.配制一定体积一定浓度的NaOH溶液时,下列操作导致结果偏高的是( )
| A. | 称量NaOH固体时动作缓慢 | B. | 定容时俯视刻度线 | ||
| C. | 定容后振荡发现液面低于刻度线 | D. | 未洗涤烧杯和玻璃棒 |
15.设NA代表阿伏加德罗常数的数值,下列说怯正确的是( )
| A. | 1mol C3H8气体中含有共价键数目为11NA | |
| B. | 1mol Na2O和Na2O2混合物中含有的阴阳离子总数是3NA | |
| C. | 将0.1mol氯化铁溶于1L水中,所得溶液含有0.1NA个Fe3+ | |
| D. | 标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为2NA |
12.下列各组离子在指定的溶液中,一定能大量共存的是( )
| A. | c(H+)=0.1mol/L的溶液:Na+、NH4+、SO42-、CO32- | |
| B. | 碱性溶液:Cu2+、NO3-、Fe3+、SO42- | |
| C. | 与铝粉反应放出H2的无色溶液:NO3-、Al3+、Na+、SO42- | |
| D. | 使红色石蕊试纸变蓝的溶液:SO42-、CO32-、Na+、K+ |
7.下列关于有机化合物的说法正确的是( )
| A. | 2-甲基丙烷(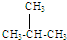 )也叫异丁烷 )也叫异丁烷 | |
| B. | 蛋白质和糖类均为天然高分子化合物 | |
| C. | 乙烯和丙烯只能发生加成反应,不能发生取代反应 | |
| D. | 苯使溴水褪色的原因是发生加成反应 |
17.金属钠露置在空气中会发生一系列变化,其中产物不可能是( )
| A. | Na2O2 | B. | NaOH | C. | Na2CO3•10H2O | D. | Na2CO3 |
4.下列电离方程式错误的是( )
| A. | Al2(SO4)3=2Al3++3SO42- | B. | NaHCO3=Na++H++CO32- | ||
| C. | Ba(OH)2=Ba2++2 OH- | D. | Na2CO3=2Na++CO32- |
1.下列物质的用途是应用其化学性质的是( )
| A. | 用铁罐储存浓硝酸 | |
| B. | 用MgO、Al2O3制作耐高温坩埚 | |
| C. | 用铁芯铝绞线作为高压输电线材料 | |
| D. | 用钠钾合金作为快中子反应堆的热交换剂 |



