题目内容
4.下列电离方程式错误的是( )| A. | Al2(SO4)3=2Al3++3SO42- | B. | NaHCO3=Na++H++CO32- | ||
| C. | Ba(OH)2=Ba2++2 OH- | D. | Na2CO3=2Na++CO32- |
分析 在书写电解质的电离方程式时,强电解质用等号,弱电解质用可逆号,多元弱酸的电离分步进行,多元弱碱的电离一步完成,据此分析.
解答 解:A、Al2(SO4)3是强电解质,在溶液中完全电离为2个铝离子和3个硫酸根,故电离方程式为Al2(SO4)3=2Al3++3SO42-,故A正确;
B、NaHCO3是强电解质,但只能完全电离为1个钠离子和1个碳酸氢根离子,故电离方程式为NaHCO3=Na++HCO3-,故B错误;
C、Ba(OH)2是强碱,能完全电离为1个钡离子和2个氢氧根离子,故电离方程式为Ba(OH)2=Ba2++2 OH-,故C正确;
D、Na2CO3是强电解质,能完全电离为2个钠离子和1个碳酸根,故电离方程式为Na2CO3=2Na++CO32-,故D正确.
故选B.
点评 本题考查了电离方程式的书写,应注意的是NaHCO3只能完全为Na+和HCO3-,而NaHSO4完全电离为Na+和H+和SO42-,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,11.2 L H2O含有的分子数为0.5NA | |
| B. | 常温常压下,11.2 L CO2 含有的分子数为0.5NA | |
| C. | 含有NA个氦原子的氦气在标准状况下的体积约为11.2 L | |
| D. | 25℃、1.01×105Pa下,64 g SO2 中含有的原子数为3NA |
7.下列说法错误的是( )
| A. | 实验室配制FeCl3溶液时,需将FeCl3 (s)溶解在较浓盐酸中,然后加水稀释 | |
| B. | 反应2CO+2NO=N2+2CO2在常温下能自发进行,则反应△H>0,△S<0 | |
| C. | 0.1mol•L-1NH4Cl溶液加水稀释,$\frac{c({H}^{+})}{c(N{H}_{4}^{+})}$的值增大 | |
| D. | 反应CH3COOCH3+H2O?CH3COOH+CH3OH△H>0,达到平衡时,加入少量固体NaOH,则乙酸甲酯水解转化率增大 |
9.下列离子方程式正确的是( )
| A. | NaHCO3溶液与NaOH溶液反应:HCO3-+OH-=CO32-+H2O | |
| B. | 少量二氧化碳通入足量的KOH溶液:CO2+OH-=HCO3- | |
| C. | Fe与稀硝酸反应产生:2Fe+6H+=2Fe3++3H2↑ | |
| D. | 氨水和醋酸溶液混合NH3•H2O+H+=NH4++H2O |
13.化学与生活密切相关.下列应用中利用了物质还原性的是( )
| A. | 明矾净水 | B. | 纯碱去油污 | ||
| C. | 焰色反应 | D. | 铁粉作食品袋内的脱氧剂 |
14.下列除去杂质的操作方法不正确的是( )
| A. | 镁粉中含少量铝粉:加足量氢氧化钠溶液充分搅拌后过滤 | |
| B. | 碳酸钠溶液中含少量碳酸氢钠:加足量澄清石灰水 | |
| C. | 氯气中混有得氯化氢气体杂质:饱和食盐水 | |
| D. | 硫酸铁溶液中混有硫酸亚铁溶液:通入氯气 |
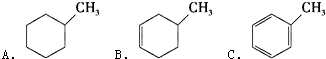
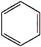 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$ +HBr.
+HBr.