题目内容
15.氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.请回答下列问题.(1)K3[Fe(CN)6]晶体中Fe3+与CN-之间的键型为配位键,该化学键能够形成的原因是CN-能提供孤对电子,Fe3+能接受孤对电子(或Fe3+有空轨道).
(2)已知:
| CH4 | SiH4 | NH3 | PH3 | |
| 沸点(K) | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度(K) | 873 | 773 | 1073 | 713.2 |
①CH4和SiH4比较,沸点高低的原因是:结构相似时,相对分子质量越大,分子间作用力越大,因此CH4的沸点低于SiH4.
②NH3和PH3比较,沸点高低的原因是:NH3分子间还存在氢键作用,因此NH3的沸点高于PH3.
分析 (1)当中心原子有空轨道,配离子含有孤对电子时,能形成配位键;
(2)①利用相对分子质量分析分子间作用力;②并注意氨气分子中有氢键.
解答 解:(1)K3[Fe(CN)6]晶体中Fe3+与CN-之间的化学键类型为配位键,Fe3+有空轨道,能接受孤对电子,CN-能提供孤对电子,所以能形成配位键,
故答案为:配位键;CN-能提供孤对电子,Fe3+能接受孤对电子(或Fe3+有空轨道);
(3)①因结构相似时,相对分子质量越大,分子间作用力越大,因此CH4的沸点低于SiH4,故答案为:结构相似时,相对分子质量越大,分子间作用力越大,因此CH4的沸点低于SiH4;
②但氨气分子间还存在氢键,则NH3的沸点高于PH3,故答案为:NH3分子间还存在氢键作用,因此NH3的沸点高于PH3.
点评 本题考查物质的结构与性质,注重对电子排布式、沸点比较、稳定性的比较及应用的考查,考查点较多,难度较大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.如图所示为冰的一种骨架形式,依此为单位向空间延伸,那么该冰中的每个水分子氢键个数为( )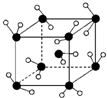

| A. | 1 | B. | 3 | C. | 2 | D. | 4 |
10.首次将量子化概念应用到原子结构,并解释了原子的稳定性的科学家是( )
| A. | 道尔顿 | B. | 爱因斯坦 | C. | 玻尔 | D. | 卢瑟福 |
4.光谱研究表明,过硫化氢溶于水时形成某一浓度的溶液中存在着下列平衡和反应:

下列判断中正确的是( )

下列判断中正确的是( )
| A. | 该溶液中存在H2S分子 | |
| B. | 该溶液中H+的浓度是S${\;}_{2}^{2-}$浓度的2倍 | |
| C. | 向该溶液中加入足量的硝酸能产生H2S气体 | |
| D. | 向该溶液中加入过量的NaOH溶液可得到含大量NaHS2的混合溶液 |

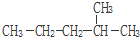 2-甲基戊烷
2-甲基戊烷  2,3-二甲基戊烷
2,3-二甲基戊烷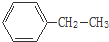 乙苯
乙苯 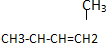 3-甲基-1-丁烯.
3-甲基-1-丁烯.