题目内容
2.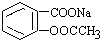 转变为
转变为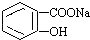 的方法是( )
的方法是( )| A. | 与足量Na0H溶液共热后,再通入CO2 | |
| B. | 溶液加热,通入足量的SO2 | |
| C. | 与稀硫酸共热后,加入足量Na0H溶液 | |
| D. | 足量稀硫酸共热后,加入足量NaHCO3 |
分析 因羧酸、酚羟基均与碱反应生成盐,则将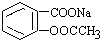 转变为
转变为 ,可选择与碱反应,然后利用碳酸酸性大于苯酚酸性,再通入二氧化碳即可;或先加稀硫酸水解后,利用苯酚酸性大于碳酸氢根离子的酸性,再与NaHCO3反应即可,以此来解答.
,可选择与碱反应,然后利用碳酸酸性大于苯酚酸性,再通入二氧化碳即可;或先加稀硫酸水解后,利用苯酚酸性大于碳酸氢根离子的酸性,再与NaHCO3反应即可,以此来解答.
解答 解:A.
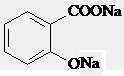 ,再通入二氧化碳气体可生成
,再通入二氧化碳气体可生成
B.亚硫酸酸性比苯甲酸强,则通入足量的SO2,不能得到羧酸钠结构,故B错误;
C.与稀硫酸共热后,加入足量的NaOH溶液,苯酚结构能与NaOH反应,则不能得到产物,故C错误;
D.与稀H2SO4共热后,酯基水解生成苯酚结构,加入足量的NaHCO3,羧基与NaHCO3反应得到产物,故D正确.
故选AD.
点评 本题考查有机物的结构和性质,根据物质的官能团变化、物质的性质选择合适的合成途径是解答本题的关键,注意碳酸酸性>苯酚酸性>碳酸氢根离子的酸性,题目难度中等.

练习册系列答案
相关题目
13.我国规定食盐的含碘量(按每千克食盐含碘元素计)为20~40mg/Kg,则每千克食盐中加入碘酸钾的物质的量应不少于(设碘酸钾的摩尔质量为M g/mol)( )
| A. | $\frac{20×1{0}^{-3}}{127}$mol | B. | 20M mol | C. | $\frac{20×1{0}^{-3}}{M}$mol | D. | $\frac{20}{M}$mol |
17.纯水在80℃时的pH( )
| A. | 等于7 | B. | 大于7 | C. | 小于7 | D. | 无法确定 |
6.Ⅰ.(1)已知某有机物A只含有C、H、O三种元素,通过元素分析知含碳54.55%,含氢9.10%.质谱分析其相对分子质量为88,经红外光谱分析其中只含C-H键和 键,其核磁共振氢谱图显示有三重峰,峰面积之比为3:2:3,该有机物不含有CH3-O-,则A的结构简式为CH3COOCH2CH3.
键,其核磁共振氢谱图显示有三重峰,峰面积之比为3:2:3,该有机物不含有CH3-O-,则A的结构简式为CH3COOCH2CH3.
(2)写出实验室制备A的化学方程式CH3COOH+HOCH2CH3$\stackrel{浓硫酸}{?}$CH3COOCH2CH3+H2O.
Ⅱ.苯甲酸甲酯 是常用香精,广泛用于食品、化妆品等行业,可从自然界中提取,也可人工合成.实验室现以食品防腐剂[主要成分为苯甲酸钠(
是常用香精,广泛用于食品、化妆品等行业,可从自然界中提取,也可人工合成.实验室现以食品防腐剂[主要成分为苯甲酸钠( )]、甲醇为原料制备苯甲酸甲酯.已知:
)]、甲醇为原料制备苯甲酸甲酯.已知:
合成苯甲酸甲酯的流程如下:

请回答下列问题:
(1)温度①约为64.7℃,操作③为分液,操作④为蒸馏.
(2)第②步加热的目的是蒸出过量的甲醇.
(3)选择合适的制备苯甲酸甲酯的装置:B.

(4)苯甲酸甲酯有多种同分异构体,写出符合下列条件的任意一种同分异构体的结构简式 .
.
①为芳香化合物 ②含有醛基 ③能与金属Na反应.
 键,其核磁共振氢谱图显示有三重峰,峰面积之比为3:2:3,该有机物不含有CH3-O-,则A的结构简式为CH3COOCH2CH3.
键,其核磁共振氢谱图显示有三重峰,峰面积之比为3:2:3,该有机物不含有CH3-O-,则A的结构简式为CH3COOCH2CH3.(2)写出实验室制备A的化学方程式CH3COOH+HOCH2CH3$\stackrel{浓硫酸}{?}$CH3COOCH2CH3+H2O.
Ⅱ.苯甲酸甲酯
 是常用香精,广泛用于食品、化妆品等行业,可从自然界中提取,也可人工合成.实验室现以食品防腐剂[主要成分为苯甲酸钠(
是常用香精,广泛用于食品、化妆品等行业,可从自然界中提取,也可人工合成.实验室现以食品防腐剂[主要成分为苯甲酸钠( )]、甲醇为原料制备苯甲酸甲酯.已知:
)]、甲醇为原料制备苯甲酸甲酯.已知:| 熔点℃ | 沸点℃ | 水溶性 | |
| 甲醇 | -97.8 | 64.7 | 易溶 |
| 苯甲酸 (一元弱酸) | 122.4 | 249.3 | 常温:0.17g 100℃:6.8g |
| 苯甲酸甲酯 | -12.3 | 198 | 难溶 |

请回答下列问题:
(1)温度①约为64.7℃,操作③为分液,操作④为蒸馏.
(2)第②步加热的目的是蒸出过量的甲醇.
(3)选择合适的制备苯甲酸甲酯的装置:B.

(4)苯甲酸甲酯有多种同分异构体,写出符合下列条件的任意一种同分异构体的结构简式
 .
.①为芳香化合物 ②含有醛基 ③能与金属Na反应.
3.高纯二氧化硅可用来制造光纤.某稻壳灰的成分为:
通过如下流程可由稻壳灰制备较纯净的二氧化硅.
(已知:AlO2-+H++H2O=Al(OH)3↓)

请回答下列问题:
(1)根据氧化物的性质进行分类,稻壳灰中涉及的氧化物最多有3类.
(2)步骤①中涉及SiO2的离子反应方程式为SiO2+2OH-=SiO32-+H2O.
(3)滤渣A的成分有Fe2O3填化学式)
(4)步骤②洗涤时,检验是否洗涤干净的方法是?:取最后一次洗涤滤液,加硝酸银溶液,若无沉淀产生,则说明洗涤干净
(5)步骤③反应的化学方程式为:H2SiO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+SiO2;实验室进行步骤③用到的仪器有坩埚钳、酒精灯、三脚架、坩埚和泥三角.
| 组分 | SiO2 | C | Na2O | K2O | Al2O3 | Fe2O3 |
| 质量分数 | 59.20 | 38.80 | 0.25 | 0.50 | 0.64 | 0.16 |
(已知:AlO2-+H++H2O=Al(OH)3↓)

请回答下列问题:
(1)根据氧化物的性质进行分类,稻壳灰中涉及的氧化物最多有3类.
(2)步骤①中涉及SiO2的离子反应方程式为SiO2+2OH-=SiO32-+H2O.
(3)滤渣A的成分有Fe2O3填化学式)
(4)步骤②洗涤时,检验是否洗涤干净的方法是?:取最后一次洗涤滤液,加硝酸银溶液,若无沉淀产生,则说明洗涤干净
(5)步骤③反应的化学方程式为:H2SiO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+SiO2;实验室进行步骤③用到的仪器有坩埚钳、酒精灯、三脚架、坩埚和泥三角.
 铁、铜及其化合物在日常生产、生活有着广泛的应用.请回答下列问题:
铁、铜及其化合物在日常生产、生活有着广泛的应用.请回答下列问题: