题目内容
(1)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式
(2)在以上中性溶液中继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式
(3)向小苏打溶液中加入过量的澄清石灰水,请写出发生反应的离子方程式 .
(2)在以上中性溶液中继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式
(3)向小苏打溶液中加入过量的澄清石灰水,请写出发生反应的离子方程式
考点:离子方程式的书写
专题:离子反应专题
分析:(1)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,NaHSO4和Ba(OH)2按照2:1反应生成硫酸钡、硫酸钠和水,以此书写离子方程式;
(2)至中性时溶液中溶质只有Na2SO4,加入Ba(OH)2溶液生成BaSO4沉淀;
(3)碳酸氢钠和过量石灰水反应,碳酸氢钠全部反应.
(2)至中性时溶液中溶质只有Na2SO4,加入Ba(OH)2溶液生成BaSO4沉淀;
(3)碳酸氢钠和过量石灰水反应,碳酸氢钠全部反应.
解答:
解:(1)NaHSO4是二元强酸的酸式盐,可以理解为全部电离.当反应后溶液呈中性时,其反应式为:2NaHSO4+Ba(OH)2=BaSO4↓+Na2SO4+2H2O,那么,
离子反应方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故答案为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O;
(2)此时溶液中溶质只有Na2SO4,加入Ba(OH)2的离子反应方程式为:Ba2++SO42-=BaSO4↓,故答案为:Ba2++SO42-=BaSO4↓;
(3)碳酸氢钠溶液中加入过量的澄清石灰水,碳酸氢钠全部反应,反应的离子方程式为:HCO3-+Ca2++OH-═CaCO3↓+H2O,
故答案为:HCO3-+Ca2++OH-═CaCO3↓+H2O.
离子反应方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故答案为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O;
(2)此时溶液中溶质只有Na2SO4,加入Ba(OH)2的离子反应方程式为:Ba2++SO42-=BaSO4↓,故答案为:Ba2++SO42-=BaSO4↓;
(3)碳酸氢钠溶液中加入过量的澄清石灰水,碳酸氢钠全部反应,反应的离子方程式为:HCO3-+Ca2++OH-═CaCO3↓+H2O,
故答案为:HCO3-+Ca2++OH-═CaCO3↓+H2O.
点评:本题考查离子方程式的书写,题目难度不大,注意根据物质的量判断反应的程度并书写相关离子方程式,注意与量有关的离子方程式的书写方法.

练习册系列答案
相关题目
下列方法对2SO2(g)+O2(g)?2SO3(g)的反应速率没有影响的是( )
| A、加入SO3 |
| B、容积不变,充入N2 |
| C、压强不变,充入N2 |
| D、降低温度 |
下列关于化学反应类型的叙述中,正确的是( )
| A、复分解反应一定不是氧化还原反应 |
| B、生成一种单质和一种化合物的反应一定是置换反应 |
| C、凡是生成盐和水的反应都是中和反应 |
| D、分解反应的生成物不一定有单质 |
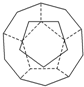 德国和美国科学家首先制出由20个碳原子组成的空心笼状分子C20,该笼状结构是由许多正五边形构成如图.
德国和美国科学家首先制出由20个碳原子组成的空心笼状分子C20,该笼状结构是由许多正五边形构成如图. A~E五种物质间的相互转化关系如图所示,其中A为单质,B为淡黄色的固体.试推断:(用化学式表示)
A~E五种物质间的相互转化关系如图所示,其中A为单质,B为淡黄色的固体.试推断:(用化学式表示)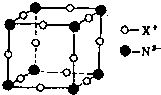 氮元素是重要的非金属元素,可形成卤化物、氮化物,叠氮化物及配合物等多种化合物.
氮元素是重要的非金属元素,可形成卤化物、氮化物,叠氮化物及配合物等多种化合物.