题目内容
下列各组试剂不用其它试剂无法鉴别的是( )
| A、MgCl2、Na2SO4、Ba(OH)2、HCl |
| B、Na2CO3、NaHCO3、Ba(OH)2、AlCl3 |
| C、NH4NO3、MgSO4、Ba(OH)2、KCl |
| D、CuSO4、K2CO3、NaCl、Ba(NO3)2 |
考点:物质的检验和鉴别的实验方案设计
专题:物质检验鉴别题
分析:首先观察溶液的颜色来鉴别物质,再根据鉴别出来的试剂向剩余溶液中滴加进行鉴别,利用不同的现象鉴别物质;若均为无色溶液,利用相互之间反应产生的不同现象鉴别,以此来解答.
解答:
解:A.一种物质与两种物质生成白色沉淀,则可鉴别出Ba(OH)2,加HCl可溶解生成的Mg(OH)2沉淀,则依次鉴别出HCl、MgCl2、Na2SO4,故A不选;
B.Ba(OH)2与三种物质均生成白色沉淀,则可鉴别出Ba(OH)2,且Ba(OH)2过量时氢氧化铝溶解,则可鉴别出AlCl3,Na2CO3、NaHCO3分别与Ba(OH)2、AlCl3的反应现象相同,不能鉴别出Na2CO3、NaHCO3,故B选;
C.Ba(OH)2与MgSO4反应生成沉淀,与NH4NO3反应生成气体,则鉴别出Ba(OH)2,然后依次得到各物质,与各物质均不反应的为KC来,故C不选;
D.蓝色溶液的为CuSO4,与CuSO4反应生成白色沉淀的为Ba(NO3)2,剩余两种与Ba(NO3)2反应生成沉淀的为K2CO3,另一物质为NaCl,故D不选;
故选B.
B.Ba(OH)2与三种物质均生成白色沉淀,则可鉴别出Ba(OH)2,且Ba(OH)2过量时氢氧化铝溶解,则可鉴别出AlCl3,Na2CO3、NaHCO3分别与Ba(OH)2、AlCl3的反应现象相同,不能鉴别出Na2CO3、NaHCO3,故B选;
C.Ba(OH)2与MgSO4反应生成沉淀,与NH4NO3反应生成气体,则鉴别出Ba(OH)2,然后依次得到各物质,与各物质均不反应的为KC来,故C不选;
D.蓝色溶液的为CuSO4,与CuSO4反应生成白色沉淀的为Ba(NO3)2,剩余两种与Ba(NO3)2反应生成沉淀的为K2CO3,另一物质为NaCl,故D不选;
故选B.
点评:本题考查物质的鉴别,为高频考点,把握物质的性质及物质之间的反应为解答的关键,注意现象与结论的关系,相同现象不能鉴别物质,综合考查元素化合物性质,题目难度中等.

练习册系列答案
相关题目
下列反应的离子方程式正确的是( )
| A、向澄清石灰水中滴加盐酸:Ca(OH)2+2H+=Ca2++2H2O |
| B、向铜粉中加入稀H2SO4:Cu+2H+=Cu2++H2↑ |
| C、向CuSO4溶液中加入Fe粉:Fe+Cu2+=Fe2++Cu |
| D、向AgNO3溶液中加入Cu粉:Ag++Cu=Cu2++Ag |
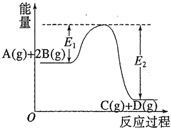 反应A(g)+2B(g)?C(g)+D(g)过程中的能量变化如图所示,有关叙述正确的是( )
反应A(g)+2B(g)?C(g)+D(g)过程中的能量变化如图所示,有关叙述正确的是( )| A、该反应是吸热反应 |
| B、当反应达到平衡时,升高温度,A的转化率增大 |
| C、反应体系中加入催化剂对反应热无影响 |
| D、在反应体系中加入催化剂,反应速率增大,E1减小,E2不变 |
决定化学反应的主要因素是( )
| A、温度 | B、压强 |
| C、浓度 | D、反应物本身的性质 |
下列各组物质的反应,能用H++OH-=H2O表示的是( )
| A、硫酸和氢氧化钡溶液 |
| B、盐酸和烧碱溶液 |
| C、硫酸和氢氧化铜 |
| D、盐酸和氢氧化铁 |
能用H++OH-=H2O来表示的化学反应是( )
| A、氢氧化铜和稀盐酸反应 |
| B、Ba(OH)2溶液中滴入稀硫酸 |
| C、KOH溶液和稀硝酸反应 |
| D、CH3COOH与NaOH溶液反应 |
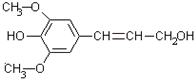 膳食纤维具有突出保健功能,近年来受到人们的普遍关注,被世界卫生组织称为人体的“第七营养素”.木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构如图,下列有关芥子醇说法正确的是( )
膳食纤维具有突出保健功能,近年来受到人们的普遍关注,被世界卫生组织称为人体的“第七营养素”.木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构如图,下列有关芥子醇说法正确的是( )| A、芥子醇的分子式是C11H12O4 |
| B、芥子醇能与FeCl3溶液发生显色反应 |
| C、芥子醇分子中所有碳原子不可能在同一平面 |
| D、1mol芥子醇能与足量溴水反应消耗1molBr2 |
下列说法中正确的是( )
| A、某无色溶液中可能含有下列离子:H+、Cl-、Na+、Fe2+ |
| B、能使石蕊变红的溶液中可能含有Cl-、K+、Na+、NO3- |
| C、取少量某溶液,向其中加入盐酸酸化的BaCl2溶液,通过观察是否有白色沉淀生成,可证明该溶液中是否含有SO42- |
| D、H++OH-═H2O可描述所有酸碱中和反应的实质 |

 和
和 