题目内容
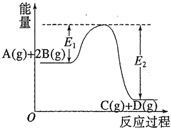 反应A(g)+2B(g)?C(g)+D(g)过程中的能量变化如图所示,有关叙述正确的是( )
反应A(g)+2B(g)?C(g)+D(g)过程中的能量变化如图所示,有关叙述正确的是( )| A、该反应是吸热反应 |
| B、当反应达到平衡时,升高温度,A的转化率增大 |
| C、反应体系中加入催化剂对反应热无影响 |
| D、在反应体系中加入催化剂,反应速率增大,E1减小,E2不变 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、图象分析可知反应物能量高于生成物,依据能量守恒分析;
B、依据图象分析反应是放热反应,升温平衡逆向进行;
C、催化剂改变反应速率不改变化学平衡;
D、催化剂同等程度改变正逆反应速率;
B、依据图象分析反应是放热反应,升温平衡逆向进行;
C、催化剂改变反应速率不改变化学平衡;
D、催化剂同等程度改变正逆反应速率;
解答:
解:A、图象分析可知反应物能量高于生成物,反应前后能量守恒,反应是放热反应,故A错误;
B、图象分析反应是放热反应,升温平衡逆向进行,A的转化率减小,故B错误;
C、催化剂改变反应速率不改变化学平衡,反应的反应热不发生变化,故C正确;
D、催化剂同等程度改变正逆反应速率,在反应体系中加入催化剂,反应速率增大,E1减小,E2减小,故D错误;
故选C.
B、图象分析反应是放热反应,升温平衡逆向进行,A的转化率减小,故B错误;
C、催化剂改变反应速率不改变化学平衡,反应的反应热不发生变化,故C正确;
D、催化剂同等程度改变正逆反应速率,在反应体系中加入催化剂,反应速率增大,E1减小,E2减小,故D错误;
故选C.
点评:本题考查了化学反应能量变化的特征分析,图象分析判断,注意催化剂改变反应速率不改变平衡的分析理解,题目较简单.

练习册系列答案
相关题目
结构简式为(CH3)2CHCH2CH(C2H5)CH(CH3)CH2CH(C2H5)CH3 的烃的名称为( )
| A、2,5-二甲基-4,7-二乙基辛烷 |
| B、2,5,7-三甲基-4-乙基壬烷 |
| C、4,7-二甲基-2,5-二乙基辛烷 |
| D、3,5,8-三甲基-6-乙基壬烷 |
将57.2g表面已锈蚀成铜绿【Cu2(OH)2CO3】的铜片投入120mL一定浓度的硝酸中,充分反应后,硝酸被还原成NO2和NO气体共8.064L(标准状况下),测得反应后溶液中c(H+)=1.0mol?L-1(假设反应前后溶液的体积不变).往反应后的溶液中加入过量NaOH溶液,滤出沉淀,经洗涤、干燥后称得质量为58.8g.则原硝酸的物质的量浓度为( )
| A、9.0 mol?L-1 |
| B、10.0 mol?L-1 |
| C、13.0 mol?L-1 |
| D、14.0 mol?L-1 |
根据元素周期表和元素周期律分析下面的推断,其中错误的是( )
| A、铍原子失电子能力比镁弱 |
| B、氢氧化钾碱性比氢氧化镁强 |
| C、硒化氢比硫化氢稳定 |
| D、碳酸比硅酸酸性强 |
下列物质转化需要加入还原剂才能实现的是( )
| A、CuO→Cu |
| B、Fe2+→Fe3+ |
| C、NaOH→NaCl |
| D、KClO3→KCl |
下列各组试剂不用其它试剂无法鉴别的是( )
| A、MgCl2、Na2SO4、Ba(OH)2、HCl |
| B、Na2CO3、NaHCO3、Ba(OH)2、AlCl3 |
| C、NH4NO3、MgSO4、Ba(OH)2、KCl |
| D、CuSO4、K2CO3、NaCl、Ba(NO3)2 |
下列有关物质分类的说法,不正确的是( )
| A、CO2是酸性氧化物,也是非金属氧化物 |
| B、KNO3是钾盐、硝酸盐,也是正盐 |
| C、H2SO4是含氧酸、二元酸,也是强酸 |
| D、NH3?H2O是一元强碱,也是可溶性碱 |
从海水中提取溴有如下反应:5NaBr+NaBrO3+3H2SO4=3Br2+3Na2SO4+3H2O,与上述反应在氧化还原原理上最相似的反应是( )
| A、2NaBr+Cl2═2NaCl+Br2 | ||||
B、2KMnO4
| ||||
| C、2H2S+SO2═3S↓+2H2O | ||||
| D、2FeCl3+H2S═2FeCl2+S↓+2HCl |
 A、B、C、D、E、F为原子序数依次增大的前20号元素,已知A有多种核素,其中一种没有中子,B和C,C和E分别相邻,D的次外层电子数是最外层电子数的两倍.B、E、F的最外层电子数之和为12.
A、B、C、D、E、F为原子序数依次增大的前20号元素,已知A有多种核素,其中一种没有中子,B和C,C和E分别相邻,D的次外层电子数是最外层电子数的两倍.B、E、F的最外层电子数之和为12.