题目内容
1.下列说法正确的是( )| A. | 乙醇、乙酸和乙酸乙酯不能用饱和Na2CO3溶液鉴别 | |
| B. | 桶烯(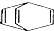 )与苯乙烯(C6H5CH=CH2)互为同分异构体,均属于芳香烃 )与苯乙烯(C6H5CH=CH2)互为同分异构体,均属于芳香烃 | |
| C. | 1.0mol的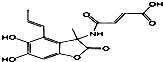 与NaOH溶液和H2反应时,分别需要消耗NaOH 6.0mol和H25.0mol 与NaOH溶液和H2反应时,分别需要消耗NaOH 6.0mol和H25.0mol | |
| D. | 按系统命名法,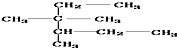 的名称为3,3-二甲基-2-乙基戊烷 的名称为3,3-二甲基-2-乙基戊烷 |
分析 A.乙醇与碳酸钠互溶,乙酸与碳酸钠反应生成气体,乙酸乙酯与碳酸钠溶液分层;
B.桶烯不含苯环;
C.2个酚-OH、1个COOC-、1个CONH-、1个-COOH及-COOC-水解生成的酚-OH与NaOH反应;苯环及2个碳碳双键与氢气发生加成反应;
D.最长的碳链含6个C,3、4号C上有甲基.
解答 解:A.乙醇与碳酸钠互溶,乙酸与碳酸钠反应生成气体,乙酸乙酯与碳酸钠溶液分层,现象不同,可鉴别,故A错误;
B.桶烯不含苯环,不属于芳香烃,但桶烯( )与苯乙烯(C6H5CH=CH2)的分子式相同结构不同互为同分异构体,故B错误;
)与苯乙烯(C6H5CH=CH2)的分子式相同结构不同互为同分异构体,故B错误;
C.2个酚-OH、1个COOC-、1个CONH-、1个-COOH及-COOC-水解生成的酚-OH与NaOH反应;苯环及2个碳碳双键与氢气发生加成反应,则1mol该有机物与NaOH溶液和H2反应时,分别需要消耗NaOH 6.0mol和H25.0mol,故C正确;
D.最长的碳链含6个C,3、4号C上有甲基,则名称为3,3,4-三甲基-己烷,故D错误;
故选C.
点评 本题考查较综合,涉及有机物的结构与性质、有机物的鉴别、命名等,为高频考点,把握有机物官能团与性质为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
12.在海水的综合利用中,海水提溴工业是一个重要组成部分,其中一种提溴的工艺是在预先浓缩并酸化的海水中,通入足量氯气,然后使生成的溴与吸收剂SO2 反应转化为氢溴酸以达到富集溴元素的目的.在有关上述工艺流程的以下化学用语中,错误的是( )
| A. | 用电子式表示氢溴酸的形成过程为: | |
| B. | 海水中Br-的电子式为: | |
| C. | 海水中通入氯气时发生反应的离子方程式为:2Br-+Cl2=Br2+2Cl- | |
| D. | Cl-的结构示意图为: |
9.青苹果(末成熟的苹果)汁遇碘变蓝色,熟的苹果汁能发生银镜反应,这说明( )
| A. | 青苹果中只含淀粉,不含糖类物质 | |
| B. | 熟的苹果中只含糖类,不含淀粉 | |
| C. | 苹果从青转熟时,淀粉水解生成单糖 | |
| D. | 苹果从青转熟时,单糖缩聚成淀粉 |
16.X+和Y2-具有与氩原子相同的电子层结构,下列叙述正确的是( )
| A. | X的原子序数比Y的小 | B. | X原子的最外层电子数比Y的大 | ||
| C. | X和Y原子的电子层数相等 | D. | X的原子半径比Y的大 |
6.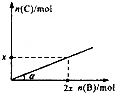 某容积可变的密闭容器中盛有足量的A,通人气体B,发生反应:A(s)+3B(g)?2C(g)+D(g);△H<0,在一定温度和压强下达到平衡.若平衡时C的物质的量与加入B的物质的量的变化关系如图所示.则下列说法中正确的是( )
某容积可变的密闭容器中盛有足量的A,通人气体B,发生反应:A(s)+3B(g)?2C(g)+D(g);△H<0,在一定温度和压强下达到平衡.若平衡时C的物质的量与加入B的物质的量的变化关系如图所示.则下列说法中正确的是( )
 某容积可变的密闭容器中盛有足量的A,通人气体B,发生反应:A(s)+3B(g)?2C(g)+D(g);△H<0,在一定温度和压强下达到平衡.若平衡时C的物质的量与加入B的物质的量的变化关系如图所示.则下列说法中正确的是( )
某容积可变的密闭容器中盛有足量的A,通人气体B,发生反应:A(s)+3B(g)?2C(g)+D(g);△H<0,在一定温度和压强下达到平衡.若平衡时C的物质的量与加入B的物质的量的变化关系如图所示.则下列说法中正确的是( )| A. | 若保持压强不变,降低温度时,图中角度a将变小 | |
| B. | 若增大压强,缩小容器的体积,平衡向正反应方向移动 | |
| C. | 若保持压强不变,再通入B,则再次达到平衡时正、逆反应速率均增大 | |
| D. | 平衡时B、C的物质的量之比为1:2 |
13.利用黄铜矿冶炼的主要原理为8CuFeS2+21O2$\frac{\underline{\;高温\;}}{\;}$8Cu+4FeO+2Fe2O3+16SO2,下列有关判断合理的是( )
| A. | 避免污染,排放的尾气用98.3%的浓硫酸吸收 | |
| B. | CuFeS2中铁显+2价,该反应中只有Cu被还原 | |
| C. | 检验炉渣中含+2价铁的试剂是盐酸、KSCN溶液和氯水 | |
| D. | 冶炼铜的废料可以冶炼铁和制硫酸 |
11.下列物质既能跟盐酸反应,又能跟NaOH溶液反应的是( )
| A. | Al2O3 | B. | NaAlO2 | C. | Mg(OH)2 | D. | NaHCO3 |
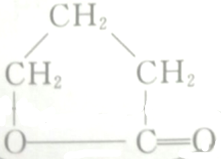 的各步反应方程式:
的各步反应方程式: