题目内容
20.用含FeS290%的硫铁矿为原料,用接触法制硫酸,如果原料的利用率为96%,硫酸的产率为90%,30t硫铁矿能生产98%的硫酸多少吨?分析 根据S元素守恒,可得关系式为:FeS2~2SO2~2SO3~2H2SO4,将每一步的损失率、利用率都归为FeS2的利用率结合关系式计算.
解答 解:设30t硫铁矿能生产98%的硫酸为x t,则:
FeS2~2SO2~2SO3~2H2SO4
120 196
30t×90%×96%×90% x t×98%
所以120:196=30t×90%×96%×90%:xt×98%
解得a=38.88
答:30t硫铁矿能生产98%的硫酸38.88吨.
点评 本题考查多步反应有损失率的计算,对多步反应计算常利用关系式进行解答,关键理解中间产物的损耗量(或转化率、利用率)都可归为起始原料的损耗量(或转化率、利用率),元素的损失率等于该化合物的损失率,难度中等.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
7.一种气态烷烃和气态烯烃组成的混合物共10g,混合气体密度是相同状况下H2密度的12.5倍,该混合气体通过溴水的试剂瓶时,试剂瓶总质量增加8.4g,该混合气体的组成可能是( )
| A. | 乙烯和乙烷 | B. | 乙烷和丙烯 | C. | 甲烷和乙烯 | D. | 丙烯和丙烷 |
8.燃烧某有机物只生成88g二氧化碳和27g水,下列说法正确的是( )
| A. | 该有机物的化学式为C3H8 | B. | 该有机物分子中一定含有碳碳双键 | ||
| C. | 该有机物不可能是乙烯 | D. | 该有机物一定含有氧元素 |
12.下列叙述正确的是( )
| A. | 卤素的氢化物中沸点最低的是HF | |
| B. | 因为H2O分子间有氢键,所以H2O比H2S稳定 | |
| C. | 一个X原子的质量为ag,则X元素的相对原子质量为aNA | |
| D. | 熔沸点:NH3<PCl3 |
9.在下列环境中,铁制品最容易生锈的是( )
| A. | 放在纯净的氧气中 | B. | 放在干燥的空气中 | ||
| C. | 放在潮湿的空气中 | D. | 浸没在蒸馏水中 |
10.下列各组混合物,不能用分液漏斗分开的是( )
①CCl4和水②乙醇和甘油③乙醛和水④苯和水⑤己烷和水⑥环己烷和苯⑦溴苯和水.
①CCl4和水②乙醇和甘油③乙醛和水④苯和水⑤己烷和水⑥环己烷和苯⑦溴苯和水.
| A. | ①②③ | B. | ②③⑥ | C. | ①④⑤⑦ | D. | ④⑤⑥ |
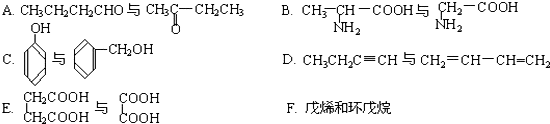
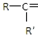 $\frac{\underline{\;氧化成\;}}{\;}$
$\frac{\underline{\;氧化成\;}}{\;}$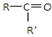 (R、R′可表示烃基或官能团),若将A中两化合物看作是某单烯烃被臭氧氧化生成的,则该单烯烃的结构简式为CH3CH2CH2CH=C(CH3)CH2CH3.
(R、R′可表示烃基或官能团),若将A中两化合物看作是某单烯烃被臭氧氧化生成的,则该单烯烃的结构简式为CH3CH2CH2CH=C(CH3)CH2CH3.