题目内容
11.将有机物A 5.4g装入元素分析装置,通入足量的O2使之完全燃烧,将生成的气体依次通过CaCl2管(a)和碱石灰(b),测得a管质量增加了3.6g,b管增加了15.4g,用质谱法测得A的谱图中分子离子峰的最大质荷比为108.(1)燃烧此有机物3.24g需消耗O2多少g?
(2)求此有机物的分子式.
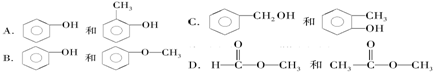
(3)该有机物1分子中有1个苯环,试写出它的同分异构体的结构简式.
分析 (1)氯化钙增加3.6g为生成水的质量,碱石灰质量增加15.4g为生成二氧化碳的质量,根据质量守恒计算5.4g消耗氧气的质量,进而计算燃烧此有机物3.24g需消耗O2的质量;
(2)计算有机物A、二氧化碳与水的物质的量,根据原子守恒计算有机物分子中N(C)、N(H),再根据有机物的相对分子质量计算分子中N(O),进而确定有机物分子式;
(3)该有机物1分子中有1个苯环,结合分子式书写可能的结构简式.
解答 解:(1)氯化钙增加3.6g为生成水的质量,碱石灰质量增加15.4g为生成二氧化碳的质量,根据质量守恒定律,则消耗O2的质量为:3.6g+15.4g-5.4g=13.6g,燃烧此有机物3.24g需消耗O2的质量为13.6g×$\frac{3.24g}{5.4g}$=8.16g,
答:燃烧此有机物3.24g需消耗O2的质量为8.16g;
(2)5.4g 有机物A的物质的量为$\frac{5.4g}{108g/mol}$=0.05mol,生成水为$\frac{3.6g}{18g/mol}$=0.2mol,生成二氧化碳为$\frac{15.4g}{44g/mol}$=0.35mol,则有机物A分子中N(C)=$\frac{0.35mol}{0.05mol}$=7,N(H)=$\frac{0.2mol×2}{0.05mol}$=8,故分子中N(O)=$\frac{108-12×7-8}{16}$=1,则A的分子式为:C7H8O,
答:有机物A的分子式为:C7H8O;
(3)有机物A的分子式为:C7H8O,分子中有1个苯环,可能的结构简式为 ,
,
答:有机物A的可能的结构简式为: ,
,
.
点评 本题考查有机物分子式确定、同分异构体书写等,掌握燃烧热利用原子守恒确定有机物分子方法,有利于基础知识的巩固.

 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案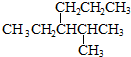 的命名正确的是( )
的命名正确的是( )| A. | 4-甲基-3-丙基戊烷 | B. | 3-异丙基己烷 | ||
| C. | 2-甲基-3-丙基戊烷 | D. | 2-甲基-3-乙基己烷 |
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
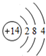 ,写出①的气态氢化物的分子式NH3.
,写出①的气态氢化物的分子式NH3.(2)元素③、⑩的最高价氧化物水化物的碱性最强的为KOH;元素②、⑧的氢化物稳定性最强的是HF;表中①-⑫化学性质最稳定的是Ar(均用化学式填空).
(3)在水溶液中⑧的单质与⑫的简单阴离子可发生反应,其离子方程式为:Cl2+2Br-=2Cl-+Br2.
(4)③、⑤两种元素的最高价氧化物的水化物的离子方程式是:Al(OH)3+OH-=AlO2-+2H2O.
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
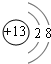 ,非金属性最强的是F.
,非金属性最强的是F.(2)①~⑩中元素的最高价氧化物对应的水化物中酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3;氢化物最稳定的是HF.
(3)按要求写出下列两种物质的电子式:⑥的氢化物
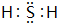 ;含有化合价为+1价的⑦的具有漂白性的一种含氧酸
;含有化合价为+1价的⑦的具有漂白性的一种含氧酸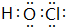 ;
;(4)在⑦与⑩对应的两种单质中,化学性质较活泼的是Cl2,可用什么化学反应证明明该事实(写出反应的化学方程式):2NaBr+Cl2=2NaCl+Br2.
| A. | 碳碳单键(CC) | B. | 碳碳双键(CC) | C. | 碳碳三键(-C≡C-) | D. | 碳氢键(CH) |
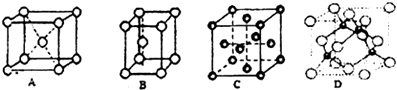
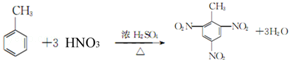
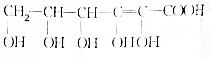 .
.
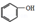 (制酚醛树脂)④
(制酚醛树脂)④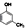 (生产杀虫剂)⑤CH2=CH─CH=CH2(合成橡胶原料)⑥HCHO(防腐剂)
(生产杀虫剂)⑤CH2=CH─CH=CH2(合成橡胶原料)⑥HCHO(防腐剂)