题目内容
13. 中和热的测量,是一个重要的定量实验.
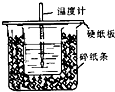
中和热的测量,是一个重要的定量实验.用50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
①从实验装置上看,图中尚缺少的一种玻璃用品是环形玻璃搅拌棒.
②大烧杯上如不盖硬纸板,求得的中和热数值偏小(填“偏大、偏小、无影响”)
③如果用60mL0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量不相等(填“相等、不相等”),所求中和热相等(填“相等、不相等”),简述理由因为中和热是指酸跟碱发生中和反应生成1molH2O所放出的热量,与酸碱的用量无关.
分析 ①根据量热计的构造来判断该装置的缺少仪器;
②大烧杯上如不盖硬纸板,会使一部分热量散失;
③反应放出的热量和所用酸以及碱的量的多少有关,并根据中和热的概念和实质来回答.
解答 解:①由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒,故答案为:环形玻璃搅拌棒;
②大烧杯上如不盖硬纸板,会使一部分热量散失,求得的中和热数值将会减小,故答案为:偏小;
③反应放出的热量和所用酸以及碱的量的多少有关,用60mL0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但是中和热的均是强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关,所以用60mL0.50mol/L盐酸进行上述实验,测得中和热数值相等;
故答案为:不相等;相等;因为中和热是指酸跟碱发生中和反应生成1molH2O所放出的热量,与酸碱的用量无关.
点评 本题考查了中和热的测定方法,题目难度中等,明确中和热的测定原理为解答关键,试题培养了学生的分析能力及化学实验能力.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
14.在密闭容器里,A与B反应生成C,其反应速率分别用vA、vB、vC表示,已知vB=3vA,3vC=2vB,则此反应可表示为( )
| A. | 2 A+3 B→2 C | B. | A+3 B→2 C | C. | 3 A+B→2 C | D. | A+B→C |
15.如图所示,甲池的总反应式O2+N2H4═2H2O+N2.有关该装置工作时,说法正确的是( )
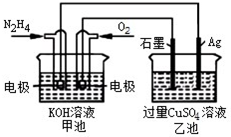

| A. | 甲池中,负极反应为N2H4-4e-═4H++N2 | |
| B. | 甲池溶液pH 保持不变,乙池溶液pH 减小 | |
| C. | 甲池中消耗2.24LO2,此时乙池中理论上多产生12.8g 固体 | |
| D. | 反应一段时间后,向乙池中加一定量CuO 固体,能使CuSO4溶液恢复到原浓度 |
8.如图曲线的变化趋势完全正确的一组是( )
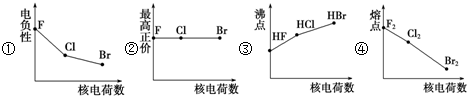

| A. | ①②③④ | B. | ②③④ | C. | ① | D. | ①②③ |
18.下列反应属于取代反应的是( )
| A. | 乙烯使溴的四氯化碳溶液褪色 | |
| B. | 苯与液溴在催化剂作用下生成溴苯 | |
| C. | 乙烯与氢气在催化剂作用下生成乙烷 | |
| D. | 乙醇在铜催化、加热条件下与氧气反应 |
5.下列解释事实的离子方程式不正确的是( )
| A. | 粗铜精炼时,阴极质量增加:Cu2++2e-═Cu | |
| B. | 明矾可用作净水剂:Al3++3H2O═Al(OH)3↓+3H+ | |
| C. | 用食醋除去水壶中的水垢(CaCO3):2CH3COOH+CaCO3═Ca2++2CH3COO-+CO2↑+H2O | |
| D. | 向氢氧化镁浊液中滴入酚酞溶液,溶液变红:Mg(OH)2(s)?Mg2+(aq)+2OH- (aq) |
2.下列说法正确的是( )
| A. | 可逆反应达到化学平衡状态时,正、逆反应的速率都为0 | |
| B. | 催化剂可以使不起反应的物质发生反应 | |
| C. | 可以找到一种催化剂使水变成油 | |
| D. | 增大反应物的浓度、提高反应温度都能增大反应速率 |
3.下列各组溶液,只用试管和胶头滴管,不用任何试剂就可以鉴别的是( )
| A. | CaCl2、Na2CO3 | B. | Ba(OH)2、NaHSO4 | C. | AlCl3、NH3•H2O | D. | Al2(SO4)3、NaOH |
