题目内容
5.已知下面表格中的数据,| 共价键 | 断开该键吸收的能量或生成该键放出的能量/kJ•mol-1 | 共价键 | 断开该键吸收的能量或生成该键放出的能量/kJ•mol-1 | 共价键 | 断开该键吸收的能量或生成该键放出的能量/kJ•mol-1 |
| H-H | 436 | H-Br | 366 | Cl-Cl | 243 |
| H-O | 463 | H-I | 298 | Br-Br | 193 |
| H-Cl | 432 | O=O | 496 | I-I | 151 |
①2H2O(g)═2H2(g)+O2(g)②H2(g)+Cl2(g)═2HCl(g)③H2(g)+Br2(g)═2HBr(g)④2HI(g)═H2(g)+I2(g)
| A. | ①④ | B. | ②③ | C. | 只有① | D. | 只有④ |
分析 根据反应的反应热△H=断键吸收的能量-成键放出的能量,若△H<0,则反应放热,若△H>0,则反应吸热,据此分析.
解答 解:①2H2O(g)═2H2(g)+O2(g)△H=断键吸收的能量-成键放出的能量=4×463KJ/mol-2×436KJ/mol-496KJ/mol=+484KJ/mol>0,故反应吸热;
②H2(g)+Cl2(g)═2HCl(g)△H=断键吸收的能量-成键放出的能量=436KJ/mol+243KJ/mol-2×432KJ/mol=-185KJ/mol<0,反应放热;
③H2(g)+Br2(g)═2HBr(g)△H=断键吸收的能量-成键放出的能量=436KJ/mol+193KJ/mol-2×366KJ/mol=-103KJ/mol<0,反应放热;
④2HI(g)═H2(g)+I2(g)△H=断键吸收的能量-成键放出的能量=2×298KJ/mol-436KJ/mol-151KJ/mol=+9KJ/mol>0,故反应吸热;
通过计算可知,①④为吸热反应,
故选A.
点评 本题考查了通过断键吸收的能量和成键放出能量的大小比较来判断反应吸放热,应注意的是△H=断键吸收的能量-成键放出的能量.

练习册系列答案
相关题目
15.在CuCl2和MgCl2的混合溶液中,加入过量的铁粉,充分反应后过滤,留在滤纸上的物质是( )
| A. | Fe | B. | Cu | C. | Fe 和 Cu | D. | Cu 和 Cu |
13.常温下,四个容积为V L的容积中分别装有质量相同的下列气体,产生的压强最大的是( )
| A. | Cl2 | B. | HCl | C. | SO2 | D. | CO2 |
20.化学键的键能是指气态基态原子间形成1mol 化学键时释放的最低能量.如:H(g)+I(g)-→H-I(g)+297kJ,即H-I键的键能为297kJ/mol,也可以理解为破坏1mol H-I键需要吸收297kJ的热量.化学反应的发生可以看成旧化学键的破坏和新化学键的形成.
表是一些键能数据(单位:kJ/mol):
阅读上述信息,回答下列问题:
(1)根据表中数据判断CCl4的稳定性小于(填“大于”或“小于”)CF4的稳定性.试预测C-Br键的键能范围:218 kJ/mol<C-Br键键能<330 kJ/mol.
(2)结合表中数据和热化学方程式H2(g)+Cl2(g)═2HCl(g)△H=-Q kJ/mol,则热化学方程式中Q的值为185.
(3)由表中数据能否得出这样的结论:
①半径越小的原子形成的共价键越牢固(即键能越大).不能(填“能”或“不能”).
②非金属性越强的原子形成的共价键越牢固.不能(填“能”或“不能”).从数据中找出一些规律,请写出一条:与相同原子结合时同主族元素形成的共价键,原子半径越小,共价键越强.
表是一些键能数据(单位:kJ/mol):
| 键能 | 键能 | 键能 | |||||
| H-H | 436 | Cl-Cl | 243 | H-Cl | 432 | ||
| S-S | 255 | H-S | 339 | C-F | 427 | ||
| C-Cl | 330 | C-I | 218 | H-F | 568 | ||
| C-O | 351 | H-O | 463 |
(1)根据表中数据判断CCl4的稳定性小于(填“大于”或“小于”)CF4的稳定性.试预测C-Br键的键能范围:218 kJ/mol<C-Br键键能<330 kJ/mol.
(2)结合表中数据和热化学方程式H2(g)+Cl2(g)═2HCl(g)△H=-Q kJ/mol,则热化学方程式中Q的值为185.
(3)由表中数据能否得出这样的结论:
①半径越小的原子形成的共价键越牢固(即键能越大).不能(填“能”或“不能”).
②非金属性越强的原子形成的共价键越牢固.不能(填“能”或“不能”).从数据中找出一些规律,请写出一条:与相同原子结合时同主族元素形成的共价键,原子半径越小,共价键越强.
17.用惰性电极电解下列各稀溶液,经一段时间后,溶液的pH值保持不变的是( )
| A. | AgNO3溶液 | B. | NaCl溶液 | C. | H2SO4溶液 | D. | K2SO4溶液 |
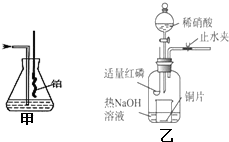 Ⅰ、实验室模拟氨催化氧化的装置如图甲:
Ⅰ、实验室模拟氨催化氧化的装置如图甲: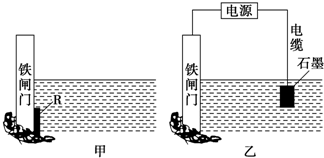 下面两个图都是金属防护的例子.
下面两个图都是金属防护的例子.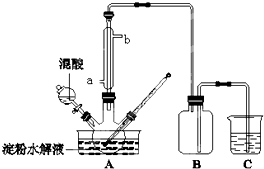 淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图所示(加热、搅拌和仪器固定装置均已略去),实验过程如下:
淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图所示(加热、搅拌和仪器固定装置均已略去),实验过程如下: