题目内容
12.下列关于厨房中的化学说法错误的是( )| A. | 用热的碱水清除炊具上残留的油污比冷的碱水清除效果好 | |
| B. | 面粉和炒菜用的花生油的主要成分均为天然高分子化合物 | |
| C. | 炒菜用过的铁锅,经放置常出现红棕色斑迹,主要发生的是电化学腐蚀 | |
| D. | 早餐经常食用的豆浆和牛奶均属于胶体,且均含有丰富的蛋白质 |
分析 A.盐类的水解是吸热反应;
B.花生油属于油脂不是高分子;
C.铁锅是铁和碳的合金;
D.豆浆和牛奶富含蛋白质.
解答 解:A.盐类的水解是吸热反应,热的碱水效果好,故A正确;
B.花生油相对分子质量较小,不是高分子化合物,故B错误;
C.铁锅是铁和碳的合金,能与空气中的水和氧气发生电化学腐蚀,故C正确;
D.豆浆和牛奶均属于胶体,富含蛋白质,故D正确.
故选B.
点评 本题考查盐类的水解、高分子化合物、电化学腐蚀以及胶体等知识,题目难度不大,掌握物质性质和相关概念是解题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.下面不能由单质直接化合而得到的化合物( )
| A. | FeCl2 | B. | AlCl3 | C. | FeS | D. | Fe3O4 |
3.琥珀酸与乙醇反应生成琥珀酸二乙酯(结构如图所示),下列有关说法正确的是( )
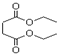

| A. | 1mol琥珀酸二乙酯能与4mol的NaOH反应 | |
| B. | 琥珀酸二乙酯在一定条件下能发生取代、加成和氧化反应 | |
| C. | 琥珀酸的分子式为C4H8O4 | |
| D. | 琥珀酸分子中含有六元环 |
20.设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A. | 78 g Na2O2中存在的共价键总数为NA | |
| B. | 0.1 mol${\;}_{38}^{90}$Sr原子中含中子数为3.8NA | |
| C. | 氢氧燃料电池负极消耗2.24 L气体时,电路中转移的电子数为0.1NA | |
| D. | 0.1 mol氯化铁溶于1L水中,所得溶液中Fe3+的数目为0.1NA |
7.用NA表示阿伏加德罗常数的数值,下列说法中不正确的是( )
| A. | 常温下,1L pH=3的硫酸溶液中,SO42-离子的数目约为5×10-4NA | |
| B. | 1mol氨基(NH2)中含有电子的数目为10NA | |
| C. | 一定条件下,1molN2与3molH2充分反应,转移电子的数目可能为2NA | |
| D. | 3molNO2和H2O完全反应,被还原的NO2分子数目为1NA |
17. 利用合成气(主要成分为CO、CO2和H2)合成甲醇,发生的主要反应如下:
利用合成气(主要成分为CO、CO2和H2)合成甲醇,发生的主要反应如下:
Ⅰ.CO(g)+2H2(g)?催化剂CH3OH(g)△H1
Ⅱ.CO2(g)+H2(g)?催化剂CO(g)+H2O(g)△H2
Ⅲ.CO2(g)+3H2(g)?催化剂CH3OH(g)+H2O(g)△H3
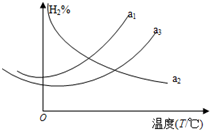
(1)上述反应达到平衡时对应的氢气的百分含量分别为a1、a2、a3,它们随温度变化的曲线如图所示.则△H2> (填“>”、“<”或“=”) 0,判断理由是升温平衡向吸热反应方向进行;△H1<△H3(填“>”、“<”或“=”).
(2)在温度T时,向某容器中充入1mol CO2和3mol H2,发生反应Ⅲ的反应.
①如果该容器为恒压容器,维持体系总压强p恒定,达到平衡时,已知H2的转化率为75%,则在该温度下平衡常数Kp=$\frac{100{P}^{2}}{3}$(用平衡分压代替平衡浓度计算,
分压=总压×物质的量分数).
②如果该容器为恒容容器,达到平衡时,H2的转化率<(填“>”、“<”或“=”)75%,理由是恒容容器中,达到平衡时体系压强比恒压容器中小.
(3)在2.0L密闭容器中放入1molCO2(g)和1molH2(g),在一定温度下发生反应Ⅱ的反应,2小时后达到平衡.下表为c(CO2)与反应时间的数据:
40min时,用CO2表示的该反应速率为0.008mol/L•min,分析该反应过程中c(CO2)变化与时间间隔(△t)的规律,得出的结论是随时间增加,二氧化碳浓度减少,反应速率减小.
 利用合成气(主要成分为CO、CO2和H2)合成甲醇,发生的主要反应如下:
利用合成气(主要成分为CO、CO2和H2)合成甲醇,发生的主要反应如下:Ⅰ.CO(g)+2H2(g)?催化剂CH3OH(g)△H1
Ⅱ.CO2(g)+H2(g)?催化剂CO(g)+H2O(g)△H2
Ⅲ.CO2(g)+3H2(g)?催化剂CH3OH(g)+H2O(g)△H3
(1)上述反应达到平衡时对应的氢气的百分含量分别为a1、a2、a3,它们随温度变化的曲线如图所示.则△H2> (填“>”、“<”或“=”) 0,判断理由是升温平衡向吸热反应方向进行;△H1<△H3(填“>”、“<”或“=”).
(2)在温度T时,向某容器中充入1mol CO2和3mol H2,发生反应Ⅲ的反应.
①如果该容器为恒压容器,维持体系总压强p恒定,达到平衡时,已知H2的转化率为75%,则在该温度下平衡常数Kp=$\frac{100{P}^{2}}{3}$(用平衡分压代替平衡浓度计算,
分压=总压×物质的量分数).
②如果该容器为恒容容器,达到平衡时,H2的转化率<(填“>”、“<”或“=”)75%,理由是恒容容器中,达到平衡时体系压强比恒压容器中小.
(3)在2.0L密闭容器中放入1molCO2(g)和1molH2(g),在一定温度下发生反应Ⅱ的反应,2小时后达到平衡.下表为c(CO2)与反应时间的数据:
| 反应时间t/min | 20 | 40 | 60 | 80 |
| c(CO2)(mol/L) | 0.300 | 0.180 | 0.109 | 0.066 |
4.下列过程中,一定需要通电才能实现的是( )
| A. | 电解质电离 | B. | 电化学防腐 | C. | 蓄电池放电 | D. | 电解精炼铜 |
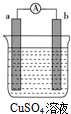 某原电池的装置如图所示,看到a极上有红色金属析出,回答下列问题:
某原电池的装置如图所示,看到a极上有红色金属析出,回答下列问题: