题目内容
1.设NA表示阿伏加德罗常数,下列说法中正确的是( )| A. | 4.4g丙烷含有碳氢键的数目为NA | |
| B. | 3.9gNa2O2与足量CO2反应转移的电子数为0.1NA | |
| C. | 标准状况下,11.2LH2O中含有的分子数为0.5NA | |
| D. | 9.2gNO2和N2O4的混合气体中含有的氮原子数为0.2NA |
分析 A.根据n=$\frac{m}{M}$计算出丙烯的物质的量,1mol丙烯中含有8mol碳氢键;
B.根据n=$\frac{m}{M}$计算出过氧化钠的物质的量,然后可计算出生成氧气的物质的,结合过氧化钠中氧元素的化合价为-1价计算转移电子数;
C.标准状况下,水的状态不是气态;
D.NO2和N2O4的最简式为NO2,根据最简式计算出混合气体中含有N原子的物质的量.
解答 解:A.4.4g丙烷的物质的量为:$\frac{4.4g}{44g/mol}$=0.1mol,0.1mol丙烷分子中含有碳氢键的物质的量为:0.1mol×8=0.8mol,含有碳氢键的数目为0.8NA,故A错误;
B.3.9g过氧化钠的物质的量为:$\frac{3.9g}{78g/mol}$=0.05mol,0.05mol过氧化钠与足量二氧化碳反应生成0.025mol氧气,反应转移电子的物质的量为:0.025mol×2=0.05mol,转移的电子数为0.05NA,故B错误;
C.标准状况下水不是气体,不能使用标准状况下的气体摩尔体积计算水的物质的量,故C错误;
D.9.2gNO2和N2O4的混合气体的最简式为NO2,含有最简式NO2的物质的量为:$\frac{9.2g}{46g/mol}$=0.2mol,含有N的物质的量为0.2mol,含有的氮原子数为0.2NA,故D正确;
故选D.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,C为易错点,注意明确标准状况下气体摩尔体积的使用条件,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
11.相同温度下,三个容器中分别盛有N2、H2、NH3.若三个容器中气体的密度相等,则下列说法中正确的是( )
| A. | 三种气体的质量相等 | |
| B. | 三种气体的物质的量之比为28:2:17 | |
| C. | 三种气体的压强之比为$\frac{1}{28}$:$\frac{1}{2}$:$\frac{1}{17}$ | |
| D. | 三个容器的容积之比为17:2:28 |
6.下列物质中熔点高低关系正确的是( )
| A. | NaCl>NaF | B. | BaO>CaO | C. | H2S>H2O | D. | SiO2>CO2 |
13.能用键能大小解释的事实是( )
| A. | 稀有气体化学性质很稳定 | B. | 硝酸易挥发,而硫酸难挥发 | ||
| C. | 氮气的化学性质比氧气稳定 | D. | 常温常压下,溴呈液态,碘呈固态 |
10.下列有关仪器使用方法或实验操作正确的是( )
| A. | 可以用酒精灯直接加热锥形瓶和容量瓶 | |
| B. | 用容量瓶配溶液时,若加水超过刻度线,立即用滴管吸出多余液体 | |
| C. | 蒸馏时温度计水银球应高于蒸馏烧瓶支管口 | |
| D. | 振荡分液漏斗时应关闭其玻璃塞和活塞 |
19.向某酸X的溶液中加人CaCO3固体.发生化学反应且生成CO2气体,下列叙述正确的是( )
| A. | CaCO3是弱电解质 | B. | CO2是弱电解质 | ||
| C. | 酸X一定是共价化合物 | D. | 酸X一定是强电解质 |
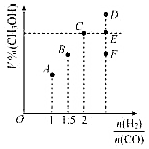 在工业上常用CO和H2合成甲醇,反应方程式为:CO(g)+2H2(g)?CH3OH(g)△H=a kJ/mol.
在工业上常用CO和H2合成甲醇,反应方程式为:CO(g)+2H2(g)?CH3OH(g)△H=a kJ/mol.