题目内容
5.一种镁原电池的反应为xMg+Mo3S4=Mgx Mo3S4;在镁原电池放电时,下列说法错误的是( )| A. | Mg2+向正极迁移 | |
| B. | 正极反应为:Mo3S4+2xe-═Mo3S${\;}_{4}^{2{x}^{-}}$ | |
| C. | Mo3S4发生氧化反应 | |
| D. | 负极反应为:xMg-2xe-═xMg2+ |
分析 在镁原电池放电时,Mg被氧化,为原电池的负极,电极反应式为xMg-2xe-=xMg2+,Mo3S4为正极反应,被还原,电极反应式为Mo3S4+2xe-=Mo3S42x-,原电池工作时,阳离子向正极移动,阴离子向负极移动,据此分析.
解答 解:A.负极生成镁离子,Mg2+向正极迁移,故A正确;
B.正极反应物质是Mo3S4,得到电子发生还原反应,正极电极反应为:Mo3S4+2xe-=Mo3S42x-,故B正确;
C.放电是原电池反应,负极反应是镁失电子发生氧化反应,正极反应物质是Mo3S4,得到电子发生还原反应,故C错误;
D.负极反应是镁失电子发生氧化反应;负极电极反应为:xMg-2xe-=xMg2+,故D正确,
故选C.
点评 本题考查了新型电池的原电池反应原理的应用,主要是依据反应元素化合价变化确定负极反应物质和 正极反应物质,书写电极反应是解题关键,题目难度中等,侧重于考查学生的分析能力和应用能力.

练习册系列答案
相关题目
15.设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,11.2 L HF中含有分子的数目为0.5 NA | |
| B. | 0.1 mol Fe与少量氯气反应生成FeCl2,转移电子数为0.2 NA | |
| C. | 1.4 g由乙烯和环丙烷组成的混合物中含有原子的数目为 0.3 NA | |
| D. | 0.1 mol•L-1碳酸钠溶液中含有CO32-离子数目小于0.1 NA |
16.化学是一门以实验为基础的自然科学,化学实验在化学学习中具有重要作用.下列关于实验的叙述中正确的有( )
| A. | 不慎碰翻燃着的酒精灯使酒精在桌面上燃烧起来,应立即用湿抺布灭火 | |
| B. | 不慎将酸沾到皮肤或衣物上,应立即用浓NaOH溶液清洗 | |
| C. | 夜间厨房发生煤气泄漏时,立即开灯检查煤气泄漏原因,并打开所有门窗通风 | |
| D. | 用氢气还原氧化铜时,先加热氧化铜,再通入氢气 | |
| E. | 可燃性气体点燃前一定要验纯 |
20.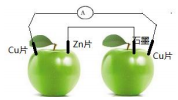 如图所示,在两个绿苹果中插入Cu片、Zn片和石墨棒,然后用导线连接,电流计指针偏转,则下列说法正确的是( )
如图所示,在两个绿苹果中插入Cu片、Zn片和石墨棒,然后用导线连接,电流计指针偏转,则下列说法正确的是( )
 如图所示,在两个绿苹果中插入Cu片、Zn片和石墨棒,然后用导线连接,电流计指针偏转,则下列说法正确的是( )
如图所示,在两个绿苹果中插入Cu片、Zn片和石墨棒,然后用导线连接,电流计指针偏转,则下列说法正确的是( )| A. | 该装置为两个原电池串联 | B. | Zn片为电源负极 | ||
| C. | 两个Cu片均不参加反应 | D. | 石墨上有O2生成 |
10.阿司匹林是一种常用的解热镇痛药,其结构如图所示,根据其结构推断,其可能有的性质为( )
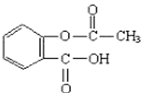

| A. | 该物质能与浓溴水发生取代反应 | B. | 该物质能发生酯化反应 | ||
| C. | 该物质属于蛋白质 | D. | 该物质极易溶于水和有机溶剂 |
17.同温同压下,相同体积的下列气体中,质量最大的是( )
| A. | 氯气 | B. | 氢气 | C. | 氧气 | D. | 氮气 |
14.过氧化钠可作为氧气的来源,常温常压下二氧化碳和过氧化钠反应后,若固体质量增加了28g,反应中有关物质的物理量正确的是(NA表示阿伏加德罗常数)( )
| 选项 | 二氧化碳 | 碳酸钠 | 转移的电子 |
| A | lmol | 2NA | |
| B | 22.4L | lmol | |
| C | 106g | lmol | |
| D | 106g | 2NA |
| A. | A | B. | B | C. | C | D. | D |
15.常温下,在固定体积为VL的密闭容器中放入1molNO气体,其压强为bKPa,若再充入1mol氧气,保持温度不变充分反应后,则反应后容积内的压强为( )
| A. | 等于2.0Kpa | B. | 等于1.5Kpa | C. | 大于1.5bKpa | D. | 小于1.5bKpa |