题目内容
下列叙述正确的是( )
| A、含1 mol H2SO4的浓硫酸中有n(H+)=2n(SO42-)=2 mol |
| B、用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液终点时仰视读数,氢氧化钠浓度偏低 |
| C、配制2.0 mol?L-1的硫酸,若定容时俯视,则所得溶液浓度偏高(其他操作均正确) |
| D、用铜电极电解2.0 mol?L-1的硫酸,阴阳两极生成气体的体积之比为2:1 |
考点:电解原理,配制一定物质的量浓度的溶液
专题:
分析:A.浓硫酸基本不电离;
B.仰视读数导致HCl体积偏大;
C.根据c=
分析;
D.用铜电极电解2.0 mol?L-1的硫酸,阳极是铜本身失电子不生成气体.
B.仰视读数导致HCl体积偏大;
C.根据c=
| n |
| V |
D.用铜电极电解2.0 mol?L-1的硫酸,阳极是铜本身失电子不生成气体.
解答:
解:A.浓硫酸基本不电离,故A错误;
B.滴定管的小刻度在下、大刻度在上,所以仰视读数导致HCl体积偏大,导致最终实验结果偏高,故B错误;
C.定容时俯视,会造成液体低于刻度线V变小,根据c=
可知,浓度偏高,故C正确;
D.用铜电极电解2.0 mol?L-1的硫酸,阳极是铜本身失电子不生成气体,故D错误;
故选C.
B.滴定管的小刻度在下、大刻度在上,所以仰视读数导致HCl体积偏大,导致最终实验结果偏高,故B错误;
C.定容时俯视,会造成液体低于刻度线V变小,根据c=
| n |
| V |
D.用铜电极电解2.0 mol?L-1的硫酸,阳极是铜本身失电子不生成气体,故D错误;
故选C.
点评:本题考查了化学实验方案评价,涉及实验误差分析,注意:A中浓硫酸基本不电离、D中用铜电极电解2.0 mol?L-1的硫酸,阳极是铜本身失电子,这些都是易错点.

练习册系列答案
相关题目
1828年,填平无机物与有机物间鸿沟的科学巨匠乌勒,他将一种无机盐直接转变为有机物尿素.乌勒使用的无机盐是尿素的同分异构体,该无机物的分子式为( )
| A、(NH4)2CO3 |
| B、NH4CNO |
| C、CH3COONH4 |
| D、NH4NO3 |
下列物质中,属于不合金的是( )
| A、水银 | B、黄铜 | C、钢铁 | D、生铁 |
某溶液中滴入KSCN溶液后变红,说明该溶液中存在( )
| A、Cl- |
| B、Fe3+ |
| C、SO42- |
| D、Mg2+ |
下列常见材料中,属于合成材料的是( )
| A、陶瓷 | B、有机玻璃 |
| C、塑料 | D、钢材 |
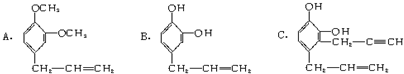
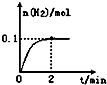 硫--碘循环分解水制氢主要涉及下列反应:
硫--碘循环分解水制氢主要涉及下列反应: