��Ŀ����
 ��--��ѭ���ֽ�ˮ������Ҫ�漰���з�Ӧ��
��--��ѭ���ֽ�ˮ������Ҫ�漰���з�Ӧ��I��SO2+2H2O+I2=H2SO4+2HI��2HI?H2+I2��2H2SO4=2SO2+O2+2H2O
��1������������Ӧ�������ж���ȷ����
a����ӦIII���ڳ����½���
b����ӦI��SO2�����Ա�HIǿ
c��ѭ���������貹��H2O
d��ѭ�������в���1molO2��ͬʱ����1molH2
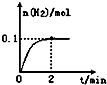
��2��һ���¶��£���1L�ܱ������м���1molHI��g����������ӦII��H2���ʵ�����ʱ��ı仯��ͼ��ʾ��
0-2min�ڵ�ƽ����Ӧ����v��HI��=
a��ƽ�ⳣ�� b��HI��ƽ��Ũ�� c���ﵽƽ���ʱ�� d��ƽ��ʱH2���������
��3��ʵ������Zn��ϡ������ȡH2����Ӧʱ��Һ��ˮ�ĵ���ƽ��
A��NaNO3 b��CuSO4 c��Na2SO4 d��NaHSO3��
���㣺��ѧƽ��ļ���,��ѧ��Ӧ���ʵ�Ӱ������
ר�⣺
��������1��a�����᳣���£����ֽ⣮
b����Ӧ�ж���������ֻ�ԭ�ԣ������Ա�HIǿ��
c��1molSO2����2molH2O����1molH2SO4��1molH2SO4�ֽ�����1molSO2��1molH2O��
d���ɢ��֪����lmolO2��ͬʱ����2molSO2����I��֪2molSO2����4molHI���ɢ��֪4molHI�ֽ�����2mol H2��
��2����ͼ��֪��2min��H2���ʵ����ı仯����Ȼ����㻯ѧ��Ӧ���ʣ������û�ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮������𣻸��ݷ�Ӧ����ʽдƽ�����ʽ�����ƽ��Ũ�ȼ���ƽ�ⳣ������ѧ����ʽ�ı䷽��ƽ�ⳣ����Ϊ����������Ũ�ȶԻ�ѧƽ���Ӱ��������HI��ƽ��Ũ�ȡ��ﵽƽ���ʱ�䡢ƽ��ʱH2��������������¶Ȳ��䣬ƽ�ⳣ�����䣻
��3��ʵ������Zn��ϡ������ȡH2���淴Ӧ����������Ũ�ȼ�С����Ӧʱ��Һ��ˮ�ĵ���ƽ��������У�����Ӱ�컯ѧ��Ӧ�������ط����ж�����Ӧ���ʵ��Լ���ע��ԭ��ط�Ӧ�ķ����жϣ�
b����Ӧ�ж���������ֻ�ԭ�ԣ������Ա�HIǿ��
c��1molSO2����2molH2O����1molH2SO4��1molH2SO4�ֽ�����1molSO2��1molH2O��
d���ɢ��֪����lmolO2��ͬʱ����2molSO2����I��֪2molSO2����4molHI���ɢ��֪4molHI�ֽ�����2mol H2��
��2����ͼ��֪��2min��H2���ʵ����ı仯����Ȼ����㻯ѧ��Ӧ���ʣ������û�ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮������𣻸��ݷ�Ӧ����ʽдƽ�����ʽ�����ƽ��Ũ�ȼ���ƽ�ⳣ������ѧ����ʽ�ı䷽��ƽ�ⳣ����Ϊ����������Ũ�ȶԻ�ѧƽ���Ӱ��������HI��ƽ��Ũ�ȡ��ﵽƽ���ʱ�䡢ƽ��ʱH2��������������¶Ȳ��䣬ƽ�ⳣ�����䣻
��3��ʵ������Zn��ϡ������ȡH2���淴Ӧ����������Ũ�ȼ�С����Ӧʱ��Һ��ˮ�ĵ���ƽ��������У�����Ӱ�컯ѧ��Ӧ�������ط����ж�����Ӧ���ʵ��Լ���ע��ԭ��ط�Ӧ�ķ����жϣ�
���
�⣺��1��a�����᳣�����¶ȣ����ֽ⣬��a����
b����Ӧ�ж���������ֻ�ԭ�ԣ���ԭ�Ա�HIǿ���ⵥ�������Դ��ڶ�������b����
c��1molSO2����2molH2O����1molH2SO4��1molH2SO4�ֽ�����1molSO2��1molH2O��ѭ����ˮ�������٣���Ӧ����ˮ����c��ȷ��
d���ɢ��֪����lmolO2��ͬʱ����2molSO2����I��֪2molSO2����4molHI���ɢ��֪4molHI�ֽ�����2mol H2����ѭ�������в���l mol O2��ͬʱ����2mol H2����d����
�ʴ�Ϊ��c��
��2����ͼ��֪2min�����������ʵ���������0.1mol����������Ũ��Ϊ
=0.1mol/L����������ʾ�Ļ�ѧ��Ӧ����Ϊ
=0.05mol/��L��min����
�ɷ�Ӧ�еĻ�ѧ��������֪v��HI��=0.05mol/��L��min����2=0.1mol/��L��min�������ݷ���ʽ����ƽ��Ũ�ȣ�c��H2��=0.1mol/L��c��I2��=0.1mol/L��c��HI��=0.8mol/L��д��ƽ�ⳣ������ʽ���㣺K=
=
=
������¶��£�H2��g��+I2��g��?2HI��g����ƽ�ⳣ��K=64��
�Ը÷�Ӧ�����¶Ȳ��俪ʼ����HI��g�������ʵ�����ԭ����2�������¶Ȳ��䣬K���䣬��a�������ʵ���Ϊԭ����2�����÷�Ӧ�Ƿ�Ӧǰ�����������ȵķ�Ӧ��
��Ӧ��ϵ�и����ʵ�Ũ�ȶ���ԭ����2������b��ȷ�����ʵ���������ѧ��Ӧ����������Ŀ죬����Ũ�ȵļ�С����������ij̶ȱ�С����c����
�ɷ�Ӧ����ʽ��ԭ��������������������ȣ�������������½�����ƽ��Ϊ��Чƽ�⣬��ƽ��ʱH2�����������ͬ����d����
�ʴ�Ϊ��0.1mol?L-1?min-1��64��b��
��3��ʵ������Zn��ϡ������ȡH2����Ӧ������������Ũ�ȼ�С����Ӧʱ��Һ��ˮ�ĵ���ƽ��������У�
���������������Լ�������������Ӧ����������
a������NaNO3 ��Һ�൱��ϡ����ҺŨ�ȼ�С����Ӧ���ʼ�С����a�����ϣ�
b������CuSO4 ��Һ����п��Ӧ����ͭ��ͭ��п��ϡ������Һ���γ�ԭ��ط�Ӧ������������������b���ϣ�
c������Na2SO4��Һ�൱��ϡ����ҺŨ�ȼ�С����Ӧ���ʼ�С����c�����ϣ�
d������NaHSO3 ��Һ���������ᣬ���������ķ�Ӧ���ʼ�С����d�����ϣ�
�ʴ�Ϊ�����ң�b��
b����Ӧ�ж���������ֻ�ԭ�ԣ���ԭ�Ա�HIǿ���ⵥ�������Դ��ڶ�������b����
c��1molSO2����2molH2O����1molH2SO4��1molH2SO4�ֽ�����1molSO2��1molH2O��ѭ����ˮ�������٣���Ӧ����ˮ����c��ȷ��
d���ɢ��֪����lmolO2��ͬʱ����2molSO2����I��֪2molSO2����4molHI���ɢ��֪4molHI�ֽ�����2mol H2����ѭ�������в���l mol O2��ͬʱ����2mol H2����d����
�ʴ�Ϊ��c��
��2����ͼ��֪2min�����������ʵ���������0.1mol����������Ũ��Ϊ
| 0.1mol |
| 1L |
| 0.1mol/L |
| 2min |
�ɷ�Ӧ�еĻ�ѧ��������֪v��HI��=0.05mol/��L��min����2=0.1mol/��L��min�������ݷ���ʽ����ƽ��Ũ�ȣ�c��H2��=0.1mol/L��c��I2��=0.1mol/L��c��HI��=0.8mol/L��д��ƽ�ⳣ������ʽ���㣺K=
| c(H 2)c(I 2) |
| c 2(HI) |
| 0.1��0.1 |
| 0��82 |
| 1 |
| 64 |
�Ը÷�Ӧ�����¶Ȳ��俪ʼ����HI��g�������ʵ�����ԭ����2�������¶Ȳ��䣬K���䣬��a�������ʵ���Ϊԭ����2�����÷�Ӧ�Ƿ�Ӧǰ�����������ȵķ�Ӧ��
��Ӧ��ϵ�и����ʵ�Ũ�ȶ���ԭ����2������b��ȷ�����ʵ���������ѧ��Ӧ����������Ŀ죬����Ũ�ȵļ�С����������ij̶ȱ�С����c����
�ɷ�Ӧ����ʽ��ԭ��������������������ȣ�������������½�����ƽ��Ϊ��Чƽ�⣬��ƽ��ʱH2�����������ͬ����d����
�ʴ�Ϊ��0.1mol?L-1?min-1��64��b��
��3��ʵ������Zn��ϡ������ȡH2����Ӧ������������Ũ�ȼ�С����Ӧʱ��Һ��ˮ�ĵ���ƽ��������У�
���������������Լ�������������Ӧ����������
a������NaNO3 ��Һ�൱��ϡ����ҺŨ�ȼ�С����Ӧ���ʼ�С����a�����ϣ�
b������CuSO4 ��Һ����п��Ӧ����ͭ��ͭ��п��ϡ������Һ���γ�ԭ��ط�Ӧ������������������b���ϣ�
c������Na2SO4��Һ�൱��ϡ����ҺŨ�ȼ�С����Ӧ���ʼ�С����c�����ϣ�
d������NaHSO3 ��Һ���������ᣬ���������ķ�Ӧ���ʼ�С����d�����ϣ�
�ʴ�Ϊ�����ң�b��
������������Ҫ�����˷�Ӧ����ʽ�ķ��������㣬��Ӧƽ��ͼ��ƽ�ⳣ������Ӧ���ʸ������Ӧ�ã��Ѷ��еȣ�����ͼ��Ҫ����ͼ��ĺ��塢�յ㡢ƽ��㣬���ƽ���ƶ����ɽ����жϣ�

��ϰ��ϵ�д�
�����Ŀ
����˵����ȷ���ǣ�������
| A��������������п��Һ��Ӧ�û�������п |
| B����������������Һ��Ӧ��������Һ������ԭ��Һ�������� |
| C���ڳ����£�����þ��������������Ӧ |
| D������ͭ���Ȼ�����Ӧ�õ������� |
����������ȷ���ǣ�������
| A����1 mol H2SO4��Ũ��������n��H+��=2n��SO42-��=2 mol |
| B������֪Ũ�ȵ�����ζ�δ֪Ũ�ȵ�����������Һ�յ�ʱ���Ӷ�������������Ũ��ƫ�� |
| C������2.0 mol?L-1�����ᣬ������ʱ���ӣ���������ҺŨ��ƫ�ߣ�������������ȷ�� |
| D����ͭ�缫���2.0 mol?L-1�����ᣬ��������������������֮��Ϊ2��1 |
���и���Һ��������÷�Һ©��������ǣ�������
| A�������ˮ | B�����Ȼ�̼��ˮ |
| C�����ͺͱ� | D���ƾ���ˮ |
����ʵ����û���õ����������ǣ�������
| A���ܽ� | B������ |
| C�������ᾧ | D����ȡ |
��������ɫ����Һ�У��ܹ�����������������ǣ�������
| A��Al3+��NO3-��K+��SO42�� |
| B��Ca2+��H+��CO32����AlO2- |
| C��OH����SO42����NH4+��Al3+ |
| D��Fe3+��Mg2+��NO3����Cl�� |
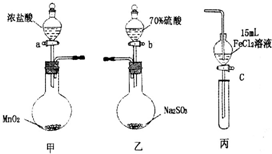 Ϊ��֤������
Ϊ��֤������