题目内容
14.标准状况下25.6g CO和CO2的混合气体的体积为17.92L,则此混合气体的平均相对分子质量为32,混合气体中CO2的物质的量为:0.2mol.分析 根据M=$\frac{m}{n}$可计算出混合气体的平均摩尔质量;设出一氧化碳和二氧化碳的物质的量,然后根据总质量、总体积列式计算出二氧化碳的物质的量即可.
解答 解:标准状况下17.92L混合气体的物质的量为:$\frac{17.92L}{22.4L/mol}$=0.8mol,该混合气体的平均摩尔质量为:$\frac{25.6g}{0.8mol}$=32g/mol,则此混合气体的平均分子质量为32;
设该混合气体中含有CO和CO2的物质的量分别为x、y,
则:28x+44y=25.6、x+y=0.8,
解得:x=0.6mol、y=0.2mol,
故答案为:32;0.2 mol.
点评 本题考查了物质的量的计算,题目难度不大,明确平均分子质量与平均摩尔质量的关系为解答关键,注意掌握物质的量与摩尔质量、气体摩尔体积之间的关系,试题培养了学生的化学计算能力.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
2.在下列四组物质的水溶液中,仅用一种化学品不能完成组内各种溶液的鉴别的是( )
| A. | Na2CO3、NaCl、AgNO3 | B. | Na2SO4、NaOH、HCl | ||
| C. | Na2SO4、NaNO3、NaOH | D. | Na2SO4、BaCl2、CuSO4 |
9.按官能团的不同可对有机物进行分类,请指出下列有机物的种类错误的一项( )
| A. | CH 3CH 2CH2 CHO醛类 | B. | 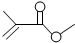 饱和酯类 饱和酯类 | ||
| C. | 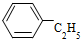 芳香烃 芳香烃 | D. | CH 3CH 2 COOH 羧酸类 |
6.下列所述事实与化学(或离子)方程式不相符的是( )
| A. | 能说明NH3结合H+能力比H2O强:NH3+H3O+=NH4++H2O | |
| B. | 能说明氧化性H2O2>Fe3+:2Fe2++H2O2+2H+=2Fe3++2H2O | |
| C. | 能说明盐酸是强酸:HCl+AgNO3=AgCl↓+HNO3 | |
| D. | 能说明CH3COOH是弱电解质:CH3COO-+H2O?CH3COOH+OH- |
5.如表是50mL稀盐酸和1g碳酸钙反应的实验数据:
分析上述数据,回答下列问题:
(1)本反应属于放热反应(填吸热或放热),实验中的所有反应,反应前后溶液的温度变化值相近(约为20℃),推测其原因是反应掉碳酸钙的量相同,放出的热量相同.
(2)实验6和7表明,温度对反应速率有影响,温度越高反应速率
越快,能表明同一规律的实验还有8和9(填实验序号).
(3)根据实验1、3、4、6、8可以得出条件对反应速率的影响规律是其它条件一定,反应物浓度越大,反应速率越快.
(4)本实验中影响反应速率的其它因素还有反应物的接触面积,能表明这一规律的实验序号是1、2与4和5.
| 实验 序号 | 碳酸钙 状态 | c(HCl) /mol•L-1 | 溶液温度/℃ | 碳酸钙消失 时间/s | |
| 反应前 | 反应后 | ||||
| 1 | 粒状 | 0.5 | 20 | 39 | 400 |
| 2 | 粉末 | 0.5 | 20 | 40 | 60 |
| 3 | 粒状 | 0.6 | 20 | 41 | 280 |
| 4 | 粒状 | 0.8 | 20 | 40 | 200 |
| 5 | 粉末 | 0.8 | 20 | 40 | 30 |
| 6 | 粒状 | 1.0 | 20 | 40 | 120 |
| 7 | 粒状 | 1.0 | 30 | 50 | 40 |
| 8 | 粒状 | 1.2 | 20 | 40 | 90 |
| 9 | 粒状 | 1.2 | 25 | 45 | 40 |
(1)本反应属于放热反应(填吸热或放热),实验中的所有反应,反应前后溶液的温度变化值相近(约为20℃),推测其原因是反应掉碳酸钙的量相同,放出的热量相同.
(2)实验6和7表明,温度对反应速率有影响,温度越高反应速率
越快,能表明同一规律的实验还有8和9(填实验序号).
(3)根据实验1、3、4、6、8可以得出条件对反应速率的影响规律是其它条件一定,反应物浓度越大,反应速率越快.
(4)本实验中影响反应速率的其它因素还有反应物的接触面积,能表明这一规律的实验序号是1、2与4和5.
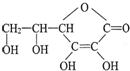 人体内的铁是以Fe2+ 和Fe3+的形式存在.正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁.服用维生素C,可使食物中的Fe3+还原成Fe2+,有利于人体吸收.
人体内的铁是以Fe2+ 和Fe3+的形式存在.正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁.服用维生素C,可使食物中的Fe3+还原成Fe2+,有利于人体吸收. .
.