题目内容
为探究CO2与NaOH溶液能发生化学反应,甲、乙、丙三位同学设计了下列三种实验装置,请回答下列问题:

(1)请写出CO2与过量的NaOH发生反应的离子方程式: .
(2)选择任意一种实验装置,简述预计出现的实验现象,解释产生该实验现象的原因.你选择的实验装置是 ,实验现象是 ,产生该实验现象的原因 .

(1)请写出CO2与过量的NaOH发生反应的离子方程式:
(2)选择任意一种实验装置,简述预计出现的实验现象,解释产生该实验现象的原因.你选择的实验装置是
考点:性质实验方案的设计,碳族元素简介
专题:实验题
分析:(1)二氧化碳和过量氢氧化钠溶液反应生成碳酸钠和水;
(2)考虑NaOH与CO2发生反应,使容器内气压变小,产生气压差分析现象.
(2)考虑NaOH与CO2发生反应,使容器内气压变小,产生气压差分析现象.
解答:
解:(1)CO2与过量的NaOH反应生成碳酸钠和水,反应的离子方程式为CO2+2OH-═CO32-+H2O,故答案为:CO2+2OH-═CO32-+H2O;
(2)选择的实验装置是甲;NaOH与CO2发生反应,使容器内气压变小,液体被压入试管中,故看到实验现象为:试管内液面上升,烧杯内的液面下降;
故答案为:甲;试管内液面上升,烧杯内的液面下降;二氧化碳和氢氧化钠溶液反应,使试管内气体压强减小,液体被压入试管中.
(2)选择的实验装置是甲;NaOH与CO2发生反应,使容器内气压变小,液体被压入试管中,故看到实验现象为:试管内液面上升,烧杯内的液面下降;
故答案为:甲;试管内液面上升,烧杯内的液面下降;二氧化碳和氢氧化钠溶液反应,使试管内气体压强减小,液体被压入试管中.
点评:本题考查化学实验方案的评价,明确二氧化碳和氢氧化钠溶液的反应的产物,装置中的压强变化是实验装置发生倒吸的原因,题目难度较小.

练习册系列答案
相关题目
工业生产中常将两种或多种金属(或金属与非金属)在同一容器中加热使其熔合,冷凝后得到具有金属特性的熔合物--合金.这是制取合金的常用方法之一.仅根据下表数据判断,不宜用上述方法制取的合金是
( )
( )
| 金属 | Na | K | Al | Cu | Fe |
| 熔点(℃) | 97.5 | 63.6 | 660 | 1083 | 1535 |
| 沸点(℃) | 883 | 774 | 2467 | 2567 | 2750 |
| A、Fe-Cu合金 |
| B、Cu-Al合金 |
| C、Al-Na合金 |
| D、Cu-Na合金 |
下列叙述正确的是( )
| A、原子晶体中只含有共价键 |
| B、离子晶体中只含有离子键,不含有共价键 |
| C、分子晶体中只存在分子间作用力,不含有其他化学键 |
| D、任何晶体中,若含有阳离子也一定含有阴离子 |
下列各组离子在水溶液中能够大量共存的是( )
| A、K+、Cl-、SO42- |
| B、SO42-、Ca2+、CO32- |
| C、H+、CO32-、Cl- |
| D、Fe3+、OH-、NO3- |


 某兴趣小组设计如图实验装置进行实验.
某兴趣小组设计如图实验装置进行实验.
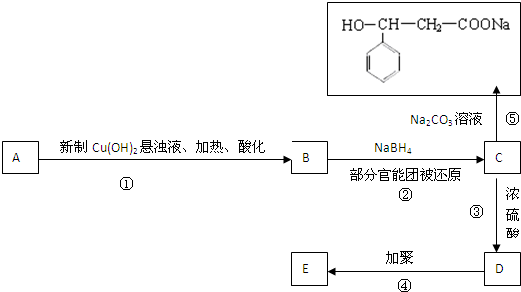
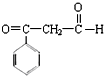 是一种重要的化工原料.A、B、C、D、E之间的转化关系如图:
是一种重要的化工原料.A、B、C、D、E之间的转化关系如图: