题目内容
在恒温、容积为2L的密闭容器中充入2mol SO2和一定量O2.发生反应2SO2+O2?2SO3,当反应进行到4min时,测得n(SO2)=0.4mol.若反应进行到2min时,容器中SO2的物质的量是( )
| A、等于1.6 mol |
| B、等于1.2 mol |
| C、大于1.6 mol |
| D、小于1.2 mol |
考点:化学平衡的计算
专题:
分析:依据化学反应速率的概念进行分析计算,并注意浓度越大,反应速率越大来解答.
解答:
解:根据化学反应速率的概念可知,进行到4min时,测得n (SO2)=0.4mol,此时反应的速率为V(SO2)=
=0.2mol/L?min;反应进行到前2min末时设二氧化硫物质的量为x,依据速率定义可得V′(SO2)=
;进行到2min时的物质浓度大于4min时的物质的浓度,所以反应时4min的反应速率小于2min的反应速率,即V′(SO2)=
>0.2mol/L?min;整理得,x<1.2mol,
故选D.
| ||
| 4min |
| ||
| 2min |
| ||
| 2min |
故选D.
点评:本题考查了化学反应速率的概念应用,化学反应速率的影响因素,主要是浓度对速率的影响判断.

练习册系列答案
相关题目
聚合硫酸铁又称聚铁,其化学式为[Fe2(OH)n(SO4)3-0.5m]x,其中n、m、x之间的关系是( )
| A、n=x(3-0.5m) |
| B、m=n+2x |
| C、m=n-6,m、n均与x无关 |
| D、n=m,m、n均与x无关 |
将铜投入稀硫酸中不能溶解,但向这种稀硫酸中加入下列某种物质后,发现铜能逐渐溶解,溶液逐渐变成蓝色,并可见有气体产生.则向这种稀硫酸中加入的物质是( )
| A、盐酸 | B、硝酸钾 |
| C、氯化钡 | D、氯化铁 |
氢化亚铜(CuH)是一难溶物质,用CuSO4溶液和“另一种反应物”在40℃~50℃时反应可生成它.CuH不稳定,易分解;CuH在氯气中能燃烧;跟盐酸反应能产生气体,以下有关它的推断中错误的是( )
| A、“另一种反应物”一定具有氧化性 |
| B、CuH既可做氧化剂也可做还原剂 |
| C、CuH+Cl2═CuCl+HCl↑(燃烧) |
| D、CuH+HCl═CuCl+H2↑(常温) |
一定量的混合气体在密闭容器中发生如下反应:mA(g)+nB(g)?pC(g),达平衡后,保持温度不变,将容器的体积缩小为原来的
,当达到新平衡时,测得C的浓度为原来的1.9倍.则下列叙述中正确的是( )
| 1 |
| 2 |
| A、m+n>p |
| B、A的转化率增大 |
| C、平衡逆向移动 |
| D、C的体积百分含量增大 |
下列有关化学反应速率的说法中正确的是( )
| A、氢气与氮气能够缓慢地反应生成氨气,使用合适的催化剂可以提高化学反应速率 |
| B、等质量的锌粉和锌片与相同体积、相同浓度的盐酸反应,反应速率相等 |
| C、用铁片与硫酸制备氢气时,浓硫酸可以加快产生氢气的速率 |
| D、增大反应CO2(g)+H2(g)═CO(g)+H2O(g)的压强,反应速率不变 |
下列各种物质放入水中能和铜起置换反应的是( )
| A、Fe(NO3)3 |
| B、AgNO3 |
| C、Fe(NO3)2 |
| D、Mg(NO3)2 |
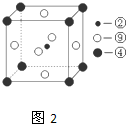 (图中②、④、⑨分别位于晶胞的体心、顶点、面心),则该化合物的化学式为
(图中②、④、⑨分别位于晶胞的体心、顶点、面心),则该化合物的化学式为 某化学兴趣小组在进行钠在空气中燃烧的实验,请写出钠在氧气中燃烧的化学方程式:
某化学兴趣小组在进行钠在空气中燃烧的实验,请写出钠在氧气中燃烧的化学方程式: