题目内容
13.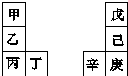 甲~辛等元素在周期表中的相对位置如表,甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素.下列判断正确的是( )
甲~辛等元素在周期表中的相对位置如表,甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素.下列判断正确的是( )| A. | 金属性:甲>乙>丁 | |
| B. | 原子半径:辛>戊>己 | |
| C. | 丙与庚的原子核外电子数相差13 | |
| D. | 乙的单质在空气中燃烧生成只含离子键的化合物 |
分析 戊的一种单质(金刚石)是自然界硬度最大的物质,则戊为C元素;甲与戊的原子序数相差3,则甲的原子序数为6-3=3,甲为Li元素;由元素在周期表中的相对位置图可知,乙为Na、丙为K、丁为Ca;丁与辛属同周期元素,由第ⅣA族元素可知,己为Si、庚为Ge、辛为Ga,然后结合元素周期律及元素化合物知识来解答.
解答 解:戊的一种单质(金刚石)是自然界硬度最大的物质,则戊为C,甲与戊的原子序数相差3,则甲的原子序数为6-3=3,即甲为Li,由元素在周期表中的相对位置图可知,乙为Na,丙为K,丁为Ca;丁与辛属同周期元素,由第ⅣA族元素可知,己为Si,庚为Ge,辛为Ga,
A.同主族,从上到下金属性增强;同周期,从左向右金属性减弱,则金属性:甲<乙<丁,故A错误;
B.电子层越多,半价越大;同主族从上到下原子半径增大,则原子半径大小为:辛>己>戊,故B错误;
C.原子序数等于核外电子数,丙(原子序数为19)与庚(原子序数为32)的原子核外电子数相差32-19=13,故C正确;
D.钠在空气中燃烧生成过氧化钠,过氧化钠中含有离子键和共价键,故D错误;
故选C.
点评 本题考查原子结构与元素周期律的关系,题目难度中等,把握金刚石的硬度及甲与戊的原子序数关系推断各元素为解答的关键,选项A中Ca的金属性比Na强为解答的易错点,注意金属活动性顺序表的应用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.如图各装置在正常工作时,都伴随有能量变化,其中由化学能转变为电能的是( )
| A. |  电解水 | B. |  太阳能热水器 | ||
| C. |  水力发电 | D. |  干电池 |
4.在一定条件下,RO3n-和I-发生反应的离子方程式为RO3n-+6I-+6H+═R-+3I2+3H2O,则RO3n-中R元素的化合价与R元素的最外层电子数分别为( )
| A. | +5,7 | B. | +5,5 | C. | +7,7 | D. | +6,6 |
1.下列叙述正确的是( )
| A. | 纯碱、烧碱均属碱 | B. | SiO2、SO2均属酸性氧化物 | ||
| C. | 凡能电离出H+的化合物均属酸 | D. | 盐类物质一定含有金属离子 |
8.下列离子方程式书写正确的是( )
| A. | NH4HCO3溶于少量的浓KOH溶液中:NH4++HCO3-+2OH-═CO32-+NH3↑+2 H2O | |
| B. | 将1mol过氧化钠投入含有1molAlCl3的溶液中:6Na2O2+6H2O+4Al3+═4Al(OH)3↓+3O2↑+12Na+ | |
| C. | NaHSO4溶液中加入Ba(OH)2溶液至溶液呈中性:Ba2++OH-+H++SO${\;}_{4}^{2-}$═BaSO4↓+H2O | |
| D. | 将16.8g 铁粉投入100mL 4.0mol/L的HNO3溶液中(还原产物只有NO)6Fe+20 H++5NO3-═3Fe2++3Fe3++5NO↑+10H2O |
18.根据有机物的结构推测,它可能发生的反应有﹙﹚

①氧化反应
②加成反应
③酯化反应
④中和反应.
①氧化反应
②加成反应
③酯化反应
④中和反应.
| A. | 只有②③④ | B. | 只有①②③ | C. | ①②③④ | D. | 只有②③ |
16.原子序数依次增大的X、Y、Z、W四种短周期元素,X、W原子的最外层电子数与其电子层数相等,X、Z的最外层电子数之和与Y、W的最外层电子数之和相等,Z为非金属性最强的元素.下列说法正确的是( )
| A. | 原子半径:W>Y>Z,而简单离子的半径:Z>Y>W | |
| B. | W的氯化物水溶液中通入XY3至过量,现象是先生成白色沉淀,后逐渐溶解 | |
| C. | Z的非金属性强于Y,因此其最高价氧化物对应水化物的酸性强于Y | |
| D. | YX3沸点远高于YZ3的原因是YX3存在分子间氢键 |
17.如表是A、B、C、D四种有机物的有关信息
回答下列问题:
(1)A与Br2的CCl4溶液反应的生成物的名称是1,2-二溴乙烷.
(2)B不能使溴水因发生化学反应而褪色,性质类似烷烃,任写一个B发生取代反应的化学方程式: +HO-NO2$→_{△}^{浓硫酸}$
+HO-NO2$→_{△}^{浓硫酸}$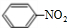 +H2O
+H2O
(3)C与Na反应的化学方程式为2CH3CH2OH+2Na→2CH3CH2ONa+H2↑.
(4)C和D反应生成相对分子质量为100的酯,该反应的反应类型为酯化反应(取代反应),其化学方程式为CH2=CH-COOH+CH3CH2OH$→_{△}^{催化剂}$CH2=CH-COOCH2CH3+H2O.
| A | ①能使溴的四氯化碳溶液褪色; ②比例模型为  ; ;③能与水在一定条件下反应生成物质C |
| B | ①由C和H两种元素组成; ②比例模型为  |
| C | ①由C、H、O三种元素组成; ②能与Na反应,但不能与NaOH溶液反应; ③能与D反应生成相对分子质量为100的酯 |
| D | ①由C、H、O三种元素组成; ②球棍模型为  |
(1)A与Br2的CCl4溶液反应的生成物的名称是1,2-二溴乙烷.
(2)B不能使溴水因发生化学反应而褪色,性质类似烷烃,任写一个B发生取代反应的化学方程式:
 +HO-NO2$→_{△}^{浓硫酸}$
+HO-NO2$→_{△}^{浓硫酸}$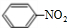 +H2O
+H2O(3)C与Na反应的化学方程式为2CH3CH2OH+2Na→2CH3CH2ONa+H2↑.
(4)C和D反应生成相对分子质量为100的酯,该反应的反应类型为酯化反应(取代反应),其化学方程式为CH2=CH-COOH+CH3CH2OH$→_{△}^{催化剂}$CH2=CH-COOCH2CH3+H2O.