题目内容
2.已知某无色溶液中存在较多的H+、SO42-、NO3-,则溶液中还可能大量存在的离子组是( )| A. | CO32-、Cl- | B. | Na+、Cu2+ | C. | Mg2+、C1- | D. | C1-、Ba2+ |
分析 溶液中存在较多的H+、SO42-、NO3-,离子之间不能结合生成沉淀、气体、水,不能发生氧化还原反应等,则离子大量共存,并结合离子的颜色来解答.
解答 解:A.H+、CO32-结合生成水和气体,不能大量共存,故A不选;
B.Cu2+为蓝色,与无色不符,故B不选;
C.该组离子之间不反应,可大量共存,且离子均为无色,故C选;
D.Ba2+、SO42-结合生成沉淀,不能大量共存,故D不选;
故选C.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,题目难度不大.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
12.下列说法或表示法正确的是( )
| A. | 等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 | |
| B. | 由C(石墨)→C(金刚石)△H=+119 kJ•mol-1可知,石墨比金刚石稳定 | |
| C. | 在稀溶液中:H++OH-═H2O△H=-57.3 kJ•mol-1,若将含1mol CH3COOH的醋酸溶液与含1 mol NaOH的溶液混合,放出的热量等于57.3 kJ | |
| D. | 在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)═2H2O(l)△H=+285.8 kJ•mol-1 |
13.10℃时,在烧杯中加入0.1mol/L的 NaHCO3溶液400mL,加热,测得该溶液的pH发生如表变化:
(1)甲同学认为,该溶液的pH升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为HCO3-+H2O?H2CO3+OH-;
(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度大于(填“大于”或“小于”)NaHCO3;
(3)丙同学设计如下实验方案对甲、乙同学的解释进行判断:
将一定体积0.1mol/L的 NaHCO3溶液置于烧杯中加热至微沸(溶液体积不变),测其pH为9.8;将烧杯冷却至室温,过一段时间(溶液体积不变)测得pH为10.1.据此可以判断乙(填“甲”或“乙”)推测正确,原因是溶液冷却至室温后pH大于8.4,说明此实验过程中有新物质生成.
| 温度(℃) | 10 | 20 | 30 | 50 | 70 |
| pH | 8.3 | 8.4 | 8.5 | 8.9 | 9.4 |
(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度大于(填“大于”或“小于”)NaHCO3;
(3)丙同学设计如下实验方案对甲、乙同学的解释进行判断:
将一定体积0.1mol/L的 NaHCO3溶液置于烧杯中加热至微沸(溶液体积不变),测其pH为9.8;将烧杯冷却至室温,过一段时间(溶液体积不变)测得pH为10.1.据此可以判断乙(填“甲”或“乙”)推测正确,原因是溶液冷却至室温后pH大于8.4,说明此实验过程中有新物质生成.
17.氢气既是最理想的能源又是重要的化工原料,用甲烷制氢气是一种廉价的制氢方法,有关的热化学方程式如下:
CH4(g)+$\frac{1}{2}$O2(g)?CO(g)+2H2(g)△H<0 ①
CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0 ①
下列说法不正确的是( )
CH4(g)+$\frac{1}{2}$O2(g)?CO(g)+2H2(g)△H<0 ①
CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0 ①
下列说法不正确的是( )
| A. | 当反应①中v正(CH4)=v逆(CO)时,表明该反应达平衡状态 | |
| B. | 其他条件不变时,增大体系压强,反应①、②中甲烷的转化率均减小 | |
| C. | 使用高效催化剂可以加快反应速率,同时提高CH4的转化率 | |
| D. | 同一容器内同时发生反应①与②时,容器内温度可能保持不变 |
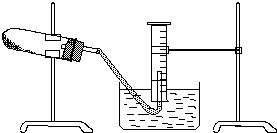 某学生用胆矾制取氧化铜固体,并研究氧化铜能否在氯酸钾受热分解实验中起催化作用.实验步骤如下:
某学生用胆矾制取氧化铜固体,并研究氧化铜能否在氯酸钾受热分解实验中起催化作用.实验步骤如下: