题目内容
3.在如右图所示的原电池中,下列说法正确的是( )
| A. | Zn为负极,Cu为正极 | B. | 正极反应式为:Zn-2e-═Zn2+ | ||
| C. | 负极反应式为:Cu-2e-═Cu2+ | D. | 该装置能将电能转化为化学能 |
分析 该原电池中,锌为负极易失电子发生氧化反应,铜为正极溶液中的氢离子在正极得电子发生还原反应,将化学能转化为电能,以此解答该题.
解答 解:A、锌比铜活泼,形成原电池时锌为负极,铜为正极,故A正确;
B、该原电池中,铜为正极溶液中的氢离子在正极得电子发生还原反应,反应式2H++2e-=H2↑,故B错误;
C、锌为负极,反应式为:Zn-2e-═Zn2+,故C错误;
D、原电池将化学能转化为电能,故D错误.
故选A.
点评 本题考查了原电池原理,为高频考点,侧重于学生的分析能力的考查,明确正负极上得失电子、电子流向即可解答,难度不大.

练习册系列答案
相关题目
14.胡椒酚的结构简式为: 下列叙述中正确的是( )
下列叙述中正确的是( )
 下列叙述中正确的是( )
下列叙述中正确的是( )| A. | 该分子中所有原子共面 | |
| B. | 该分子可与FeCl3溶液反应呈紫色 | |
| C. | 1mol该物质最多可与4molH2发生反应 | |
| D. | 1mol该分子最多可与4mol溴发生反应 |
11.某同学用图中四种装置从海带里提取取碘,其中正确且能达到实验目的是( )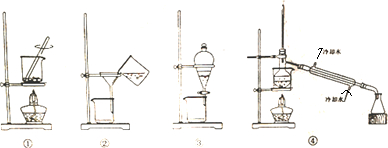

| A. | 装置①将海带灼烧成灰 | B. | 装置②过滤含I-的溶液 | ||
| C. | 装置③放出碘的CCl4溶液 | D. | 装置④分离碘并回收CCl4 |
18.在同温同压下,下列各组热化学方程式中,△H1>△H2的是( )
| A. | 2H2(气)+O2(气)═2H2O(气)△H1 2H2(气)+O2(气)═2H2O(液)△H2 | |
| B. | S(气)+O2(气)═SO2(气)△H1 S(固)+O2(气)═SO2(气)△H2 | |
| C. | C(固)+O2(气)═CO2(气)△H1 C(固)+$\frac{1}{2}$O2 (气)═CO(气)△H2 | |
| D. | H2(气)+Cl2(气)═2HCl(气)△H1 $\frac{1}{2}$H2(气)+$\frac{1}{2}$Cl2(气)═HCl(气)△H2 |
8.25℃,向20mL 0.1mol•L-1的H3PO2溶液中滴加0.1mol•L-1的NaOH溶液(滴定过程中溶液温度保持不变),滴定曲线如图1,含磷物种浓度所占分数(δ)随pH变化关系如图2,则下列说法不正确的是( )

| A. | H3PO2的电离方程式为:H3PO2?H2PO2-+H+;电离常数Ka≈10-5 | |
| B. | B点溶液中存在关系:2c(H+)+c(H3PO2)=2c(OH-)+c(H2PO2-) | |
| C. | 图2中的a点对应为 图1中的B点 | |
| D. | D点时,溶液中微粒浓度大小关系为:c(Na+)>c(H2PO2-)>c(OH-)>c(H+) |
12.对下列有机反应类型的认识,错误的是( )
| A. | CH3CH2OH+CH3COOH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;酯化反应 | |
| B. | CH2=CHCH3+Br2$\stackrel{光照}{→}$CH2=CHCH2Br+HBr;加成反应 | |
| C. | 2CH3CH2OH+O2→2CH3CHO+2H2O;氧化反应 | |
| D. |  +Br2$\stackrel{FeBr_{3}}{→}$ +Br2$\stackrel{FeBr_{3}}{→}$ +HBr;取代反应 +HBr;取代反应 |