题目内容
14.胡椒酚的结构简式为: 下列叙述中正确的是( )
下列叙述中正确的是( )| A. | 该分子中所有原子共面 | |
| B. | 该分子可与FeCl3溶液反应呈紫色 | |
| C. | 1mol该物质最多可与4molH2发生反应 | |
| D. | 1mol该分子最多可与4mol溴发生反应 |
分析 分子中含有酚羟基,可发生取代、氧化和颜色反应,含有碳碳双键,可发生加成、加聚和氧化反应,以此解答该题.
解答 解:A.分子中含有CH2原子团,具有甲烷的结构特点,所有原子不可能在同一个平面上,故A错误;
B.含有酚羟基,可与FeCl3溶液反应呈紫色,故B正确;
C.能与氢气发生加成反应的为苯环和碳碳双键,则1mol该物质最多可与4molH2发生反应,故C正确;
D.分子中含有1个酚羟基,有2个邻位氢原子可被取代,且碳碳双键可与溴发生加成反应,则1mol胡椒酚最多可与3mol溴发生反应,故D错误.
故选BC.
点评 本题考查有机物的结构和性质,为高考常见题型和高频考查,侧重于学生的分析能力的考查,注意把握有机物的结合特点和官能团的性质,为解答该题的关键,难度不大.

练习册系列答案
相关题目
5.硼酸(H3BO3)大量应用于玻璃制造行业,以硼镁矿(2MgO•B2O3•H2O、SiO2及少量Fe3O4、CaCO3,Al2O3)为原料生产硼酸的工艺流程如图1:

已知:H3BO3在20℃、40℃、60℃、100℃时的溶解度依次为5.0g、8.7g、14.8g、40.2g.Fe3+、Al3 +、Fe2+和Mg2 +以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2、9.7和 12.4.
(1)由于矿粉中含CaCO3,为防止“浸取”时容易产生大量泡沫使物料从反应器中溢出,应采取的措施是:分批慢慢加入稀硫酸.
(2)“浸出液”显酸性,含H3BO3和Mg2+和SO42-,还含有Fe2+、Fe3+、Ca2+、Al3+等杂质.“除杂”时向浸出液中依次加入适量H2O2和MgO,除去的杂质离子是Fe3+、Fe2+、Al3+.H2O2的作用是H2O2+2H++2Fe2+=2Fe3++2H2O (用离子方程式表示).
(3)“浸取”后,采用“热过滤”的目的是防止温度下降时H3BO3从溶液中析出.
(4)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图2,且溶液的沸点随压强增大而升高.为了从“母液”中充分回收MgSO4•H20,应采取的 措施是将“母液”蒸发浓缩,加压升温结晶
(5)已知298K时,硼酸(H3BO3)溶液中存在如下反应:H3BO3(aq)+H2O(l)?[B(OH)4]-(aq)+H+(aq) K=5.7×10-10
下列说法正确的是BD.
A.碳酸钠溶液滴入硼酸中能观察到有气泡产生
B.碳酸钠溶液滴入醋酸中能观察到有气泡产生
C.等浓度的碳酸和硼酸溶液比较,pH:前者>后者
D.等浓度的碳酸钠和醋酸钠溶液比较,pH:前者>后者.

已知:H3BO3在20℃、40℃、60℃、100℃时的溶解度依次为5.0g、8.7g、14.8g、40.2g.Fe3+、Al3 +、Fe2+和Mg2 +以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2、9.7和 12.4.
(1)由于矿粉中含CaCO3,为防止“浸取”时容易产生大量泡沫使物料从反应器中溢出,应采取的措施是:分批慢慢加入稀硫酸.
(2)“浸出液”显酸性,含H3BO3和Mg2+和SO42-,还含有Fe2+、Fe3+、Ca2+、Al3+等杂质.“除杂”时向浸出液中依次加入适量H2O2和MgO,除去的杂质离子是Fe3+、Fe2+、Al3+.H2O2的作用是H2O2+2H++2Fe2+=2Fe3++2H2O (用离子方程式表示).
(3)“浸取”后,采用“热过滤”的目的是防止温度下降时H3BO3从溶液中析出.
(4)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图2,且溶液的沸点随压强增大而升高.为了从“母液”中充分回收MgSO4•H20,应采取的 措施是将“母液”蒸发浓缩,加压升温结晶
(5)已知298K时,硼酸(H3BO3)溶液中存在如下反应:H3BO3(aq)+H2O(l)?[B(OH)4]-(aq)+H+(aq) K=5.7×10-10
| 化学式 | 碳酸 | 醋酸 |
| 电离常数 | K1=4.4×10-7K2=4.7×10-11 | K=1.75×10-5 |
A.碳酸钠溶液滴入硼酸中能观察到有气泡产生
B.碳酸钠溶液滴入醋酸中能观察到有气泡产生
C.等浓度的碳酸和硼酸溶液比较,pH:前者>后者
D.等浓度的碳酸钠和醋酸钠溶液比较,pH:前者>后者.
9.关于甲醇碱性燃料电池的叙述正确的是( )
| A. | 加入甲醇的电极是电池的正极 | |
| B. | 电池工作时氧气发生氧化反应 | |
| C. | 电池负极反应式为O2+4H++4e-═2H2O | |
| D. | 电池工作后电解质溶液碱性减弱 |
6. 化学反应的快慢和限度对人类生产生活有重要的意义.
化学反应的快慢和限度对人类生产生活有重要的意义.
(1)将反应速率的影响条件填在空格处.
(2)800℃时,A、B、C三种气体在固定体积的密闭容器中反应,反应过程中各物质的浓度变化如图所示,分析图象回答问题:
①该反应的化学方程式为2A?2B+C;
(2)2min内,用C表示的反应速率为0.05mol/(L•min).
③在其他条件下,测得A的反应速率为0.05mol•L-1•min-1,此时的反应与800b℃时相比.
a.比800℃时快 b.比800℃时慢 c.与800℃时速率相等 d.无法确定
(3)判断该反应达到平衡状态的标志是ce
a.A和B的浓度相等
b.v(B)=2v(C)
c.容器内气体压强不再改变
d.密闭容器中混合气体的密度不变
e.容器内A的体积分数不再改变.
 化学反应的快慢和限度对人类生产生活有重要的意义.
化学反应的快慢和限度对人类生产生活有重要的意义.(1)将反应速率的影响条件填在空格处.
| 实例 | 影响条件 |
| ①食物放在冰箱里能延长保质期 | |
| ②工业炼铁时,把铁矿石预先粉碎后,再进行炼制 | |
| ③用H2O2分解制O2,加入MnO2 |
①该反应的化学方程式为2A?2B+C;
(2)2min内,用C表示的反应速率为0.05mol/(L•min).
③在其他条件下,测得A的反应速率为0.05mol•L-1•min-1,此时的反应与800b℃时相比.
a.比800℃时快 b.比800℃时慢 c.与800℃时速率相等 d.无法确定
(3)判断该反应达到平衡状态的标志是ce
a.A和B的浓度相等
b.v(B)=2v(C)
c.容器内气体压强不再改变
d.密闭容器中混合气体的密度不变
e.容器内A的体积分数不再改变.
3.在如右图所示的原电池中,下列说法正确的是( )


| A. | Zn为负极,Cu为正极 | B. | 正极反应式为:Zn-2e-═Zn2+ | ||
| C. | 负极反应式为:Cu-2e-═Cu2+ | D. | 该装置能将电能转化为化学能 |
4.下列4种烯烃分别经催化加氢后不能得到2甲基戊烷的是( )
| A. |  | B. |  | C. |  | D. |  |

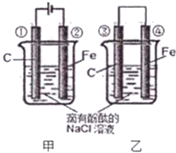 化学能和电能的相互转化是能量转化的重要形式,电池在现代生活的很多方面得到广泛应用.
化学能和电能的相互转化是能量转化的重要形式,电池在现代生活的很多方面得到广泛应用.