题目内容
15.用某仪器量一液体体积时,平视时体积为V1mL,仰视读数为V2ml,俯视读数为V3mL,若V3>V1>V2,则所使用的仪器可能是( )| A. | 容量瓶 | B. | 量筒 | C. | 碱式滴定管 | D. | 以上仪器均可 |
分析 仰视读数读出的是下面的刻度,俯视读数时读出的是上面的刻度,据此分析.
解答 解:A、容量瓶只有一条刻度线,且不能用于量取液体的体积,故A错误;
B、量筒可以用于量取液体的体积,且量筒越往上刻度越大,故央视时刻度偏小,俯视时刻度偏大,故B正确;
C、碱式滴定管可以用于量取液体的体积,但滴定管的0刻度在上,故越往下刻度越大,则俯视时读数偏小,仰视时刻度偏大,故C错误;
D、此仪器可以是量筒,故D错误.
故选B.
点评 本题考查常计量仪器的构造及其使用方法,题目难度不大,注意明确计量仪器的构造解题的关键,试题注重了基础知识的考查.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.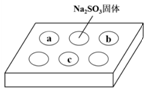 某同学进行SO2的性质实验.在点滴板a、b、c处分别滴有不同的试剂,再向Na2S
某同学进行SO2的性质实验.在点滴板a、b、c处分别滴有不同的试剂,再向Na2S
O3固体上滴加数滴浓H2SO4后,在整个点滴板上盖上培养皿,一段时间后观察到的实验现象如表所示.下列说法正确的是( )
 某同学进行SO2的性质实验.在点滴板a、b、c处分别滴有不同的试剂,再向Na2S
某同学进行SO2的性质实验.在点滴板a、b、c处分别滴有不同的试剂,再向Na2SO3固体上滴加数滴浓H2SO4后,在整个点滴板上盖上培养皿,一段时间后观察到的实验现象如表所示.下列说法正确的是( )
| 序号 | 试剂 | 实验现象 |
| a | 品红溶液 | 红色褪去 |
| b | 酸性KMnO4溶液 | 紫色褪去 |
| c | NaOH溶液(含2滴酚酞) | 红色褪去 |
| A. | 浓硫酸与Na2SO3固体发生了氧化还原反应 | |
| B. | a、b均表明SO2具有漂白性 | |
| C. | c中只可能发生反应:SO2+2OH-═SO32-+H2O | |
| D. | c中所得溶液的离子浓度一定存在关系:c(Na+)+c(H+)=2c(SO32-)+c(HSO3-)+c(OH-) |
10.室温下,关于1.0mL 0.l mol/L氨水,下列判断正确的是( )
| A. | 溶液的pH等于13 | |
| B. | 加入少量NH4Cl固体,c(OH-)不变 | |
| C. | c(OH-)=c(NH4+)+c(H+) | |
| D. | 与1.0 mL 0.l mol/L盐酸混合后,溶液呈中性 |
20.目前世界上用量最大,用途最广的合金是( )
| A. | 铝合金 | B. | 青铜 | C. | 钢铁 | D. | 塑钢 |
7.密闭容器中分别盛有以下各选项的物质,其中一定为纯净物的是( )
| A. | 二氟甲烷 | B. | 二溴乙烷 | C. | 二甲基苯 | D. | 2-丁烯 |
4.下列各组分子中,都属于含极性键的非极性分子的是( )
| A. | CO2 H2S | B. | C2H4 BF3 | C. | C60 C2H4 | D. | NH3 HCl |
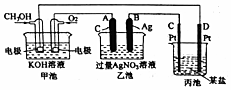
 将镁、铝的混合物共0.1mol,溶于200mL 2.5mol•L-1的盐酸溶液中,然后再滴加2mol•L-1的NaOH溶液.请回答下列问题:
将镁、铝的混合物共0.1mol,溶于200mL 2.5mol•L-1的盐酸溶液中,然后再滴加2mol•L-1的NaOH溶液.请回答下列问题: