��Ŀ����
2����ҵ������������Ҫ�ɷ�ΪAl2O3��������Fe2O3��SiO2��Ϊԭ��ұ����������ͼ��ʾ��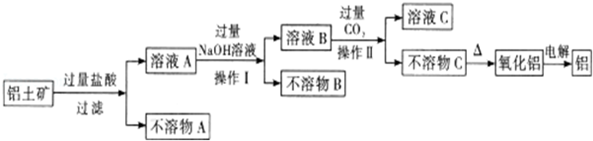
�Իش��������⣺
��1��ʵ����������õ��IJ����������ձ���©������������
��2��������A��SiO2���ѧʽ����ͬ����������B��Fe��OH��3��
��3��д������������������Ӧ�����ӷ���ʽAl3++4OH-=AlO2-+2H2O��Fe3++3OH-=Fe��OH��3����д�����ɲ�����C�����ӷ���ʽAlO2-+CO2+2H2O=Al��OH��3��+HCO3-
��4�����������۵�ߴ�2054�棬��ҵ��Ϊ�����ܺģ������ĵ��ұ��ʱ����ȡ�Ĵ�ʩ�Ǽ������ʯ�����������۵㣮
���� ��������Ҫ�ɷ�ΪAl2O3��������Fe2O3��SiO2���м�������ϡ���ᣬ�����ķ�ӦΪAl2O3+6H+=2Al3++3H2O��Fe2O3+6H+=2Fe3++3H2O��SiO2��ϡ�����Ӧ��Ȼ����ˣ�������ҺA������ΪFeCl3��AlCl3��HCl��������AΪSiO2����A��Һ�м������NaOH��Һ�����������ӷ�ӦΪFe3++3OH-=Fe��OH��3����Al3++4OH-=AlO2-+2H2O��Ȼ����ˣ���ҺB�к���NaAlO2��NaOH��������BΪFe��OH��3������ҺB��ͨ������������̼�����������ӷ�Ӧ����ʽΪOH-+CO2=HCO3-��AlO2-+CO2+2H2O=Al��OH��3��+HCO3-��Ȼ����ˣ��õ�����ҺC������ΪNaHCO3��������C��Al��OH��3������Al��OH��3�������ķ�ӦΪ��2Al��OH��3$\frac{\underline{\;\;��\;\;}}{\;}$Al2O3+3H2O����������������õ�Al���ݴ˷����ش����⣮
��� �⣺��������Ҫ�ɷ�ΪAl2O3��������Fe2O3��SiO2���м�������ϡ���ᣬ�����ķ�ӦΪAl2O3+6H+=2Al3++3H2O��Fe2O3+6H+=2Fe3++3H2O��SiO2��ϡ�����Ӧ��Ȼ����ˣ�������ҺA������ΪFeCl3��AlCl3��HCl��������AΪSiO2����A��Һ�м������NaOH��Һ�����������ӷ�ӦΪFe3++3OH-=Fe��OH��3����Al3++4OH-=AlO2-+2H2O��Ȼ����ˣ���ҺB�к���NaAlO2��NaOH��������BΪFe��OH��3������ҺB��ͨ������������̼�����������ӷ�Ӧ����ʽΪOH-+CO2=HCO3-��AlO2-+CO2+2H2O=Al��OH��3��+HCO3-��Ȼ����ˣ��õ�����ҺC������ΪNaHCO3��������C��Al��OH��3������Al��OH��3�������ķ�ӦΪ��2Al��OH��3$\frac{\underline{\;\;��\;\;}}{\;}$Al2O3+3H2O����������������õ�Al��
��1��ʵ����������õ��IJ����������ձ�����������©�����ʴ�Ϊ��©������������
��2������������֪������A��SiO2��������B��ΪFe��OH��3���ʴ�Ϊ��SiO2��Fe��OH��3��
��3������������������ӦΪ��Fe3++3OH-=Fe��OH��3����Al3++4OH-=AlO2-+2H2O�������������ɲ�����C�����ӷ���ʽ�ǣ�AlO2-+CO2+2H2O=Al��OH��3��+HCO3-��
�ʴ�Ϊ��Fe3++3OH-=Fe��OH��3����Al3++4OH-=AlO2-+2H2O��AlO2-+CO2+2H2O=Al��OH��3��+HCO3-��
��4�����������۵�ߴ�205�棬��ҵ��Ϊ�����ܺģ������ĵ��ұ��ʱ����ȡ�Ĵ�ʩ�Ǽ������ʯ�����������۵㣬
�ʴ�Ϊ���������ʯ�����������۵㣮
���� �����������仯����Ϊ���忼�����ʷ�����ᴿ���ۺ��Խ�ǿ���漰���ӷ���ʽ����д�������ƶϡ�����ұ��������������֪ʶ�㣬��ȷ������������������;�����ӷ���ʽ��д�����ԭ����֪ʶ�㼴�ɽ����Ŀ�Ѷ��еȣ�

| A�� | ��֬�����������Է��������ܴ����ڸ߷��ӻ����� | |
| B�� | ���۷�Ӧ�ĵ����������������� | |
| C�� | ���Ը߷��ӵij����Ͽ��Դ�֧�� | |
| D�� | ��ľ���������� |
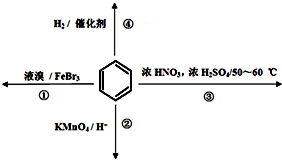
| A�� | ��Ӧ�ٳ����²��ܽ��� | |
| B�� | ��Ӧ�ڲ��������������зֲ�������ɫ�����²� | |
| C�� | ��Ӧ��Ϊ�ӳɷ�Ӧ | |
| D�� | ��Ӧ���ܷ������Ӷ�֤�������ǵ�˫������ṹ |
| A�� | �����ձ������۾�����ȫ�ܽ⣬�����ձ��зų�����������ͬ | |
| B�� | �����ձ������۾�δ��ȫ�ܽ⣬��ʢ����������Һ���ձ��зų������������� | |
| C�� | ����Ӧ����һ���ձ���������ȫ�ܽ⣬��һ���ձ�������û����ȫ�ܽ⣬���Ǹ�������û���ܽ���ձ�ԭ��ʢ�ŵ�������������Һ | |
| D�� | ������Σ����������۷�Ӧ������H2�����ܱ�����������Һ�����۷�Ӧ������H2�� |
| A�� | ��ˮ��������ɫ��ƿ�У��Ᵽ�����������ǵ��Լ�ƿ�� | |
| B�� | �����ƺ�����FeCl3��Һʱ��Ҫ�����������ۣ��Է��ڿ����б��� | |
| C�� | �ռ����ȼ�����ҺӦ���������в��������Լ�ƿ�� | |
| D�� | Ư�ۡ��ռNa2SiO3��Ҫ�ܷⱣ�� |
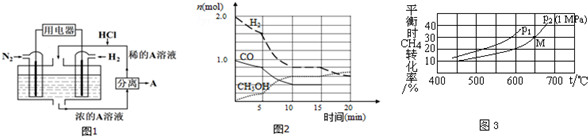
 ��
�� ���ᾧ�����ɿ���H2C2O4•xH2O��ʾ��Ϊ�˲ⶨxֵ����������ʵ�飺��ȡWg���ᾧ�壬���100mLˮ��Һ����ȡ25.00mL�����ƵIJ�����Һ������ƿ�ڣ���������ϡH2SO4����Ũ��Ϊamol•L-1��KMnO4��Һ�ζ����������ķ�Ӧ��KMnO4+H2C2O4+H2SO4=K2SO4+CO2��+MnSO4+H2O
���ᾧ�����ɿ���H2C2O4•xH2O��ʾ��Ϊ�˲ⶨxֵ����������ʵ�飺��ȡWg���ᾧ�壬���100mLˮ��Һ����ȡ25.00mL�����ƵIJ�����Һ������ƿ�ڣ���������ϡH2SO4����Ũ��Ϊamol•L-1��KMnO4��Һ�ζ����������ķ�Ӧ��KMnO4+H2C2O4+H2SO4=K2SO4+CO2��+MnSO4+H2O