题目内容
5. X、Y、Z三种短周期元素在周期表中的位置如图,其中Z单质可用于工业制漂白粉,下列说法不正确的是( )
X、Y、Z三种短周期元素在周期表中的位置如图,其中Z单质可用于工业制漂白粉,下列说法不正确的是( )| A. | Y的非金属性比Z的弱 | |
| B. | 三种元素均为非金属元素 | |
| C. | Z形成的气态氢化物比Y形成的气态氢化物稳定 | |
| D. | Y元素的最高正化合价比Z元素的最高正化合价高 |
分析 X、Y、Z三种短周期,其中Z单质可用于工业制漂白粉,则Z为Cl元素;由元素在周期表中的位置可知,X为N,Y为S,然后结合元素周期律及元素化合物知识来解答.
解答 解:X、Y、Z三种短周期,其中Z单质可用于工业制漂白粉,则Z为Cl元素;由元素在周期表中的位置可知,X为N,Y为S,
A.同周期从左向右非金属性增强,则Y的非金属性比Z的弱,故A正确;
B.N、S、Cl均为非金属元素,故B正确;
C.非金属性越强,对应氢化物越稳定,则Z形成的气态氢化物比Y形成的气态氢化物稳定,故C正确;
D.Y元素的最高正化合价为+6,Z元素的最高正化合价为+7,故D错误;
故选D.
点评 本题考查元素位置、结构与性质的关系,为高频考点,把握元素的位置、元素的性质及元素周期律为解答的关键,侧重分析与应用能力的考查,注意Z为Cl为元素推断的突破口,题目难度不大.

练习册系列答案
相关题目
15.下列说法正确的是( )
| A. | 只用水就可以鉴别四氯化碳、苯和乙醇 | |
| B. | C2H4、C3H6、C6H6分子中,所有原子处于同一平面上 | |
| C. | 光照条件下,氯气与乙烷发生化学反应,生成的产物有6种 | |
| D. | 有机物 与氯气发生取代反应,生成的一氯代物有5种 与氯气发生取代反应,生成的一氯代物有5种 |
13.如表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题.
(1)非金属性最强的元素是F(填元素符号,下同),形成化合物种类最多的元素是C.
(2)第三周期元素除⑩外原子半径最小的是Cl(填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是NaOH(填化学式,下同),具有两性的是Al(OH)3.
(3)⑤⑥⑦单质的活泼性顺序为Na>Mg>Al(填元素符号),判断的实验依据是单质与水或酸反应的剧烈程度(写出一种).
(4)⑧和⑨非金属性较强的是Cl,试用化学反应方程式说明Cl2+Na2S═2NaCl+S↓.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)第三周期元素除⑩外原子半径最小的是Cl(填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是NaOH(填化学式,下同),具有两性的是Al(OH)3.
(3)⑤⑥⑦单质的活泼性顺序为Na>Mg>Al(填元素符号),判断的实验依据是单质与水或酸反应的剧烈程度(写出一种).
(4)⑧和⑨非金属性较强的是Cl,试用化学反应方程式说明Cl2+Na2S═2NaCl+S↓.
20.下列实验中,能证明苯酚的酸性极弱的是( )
| A. | 跟氢氧化钠溶液反应生成苯酚钠 | |
| B. | 跟FeCl3溶液作用显紫色 | |
| C. | 常温下苯酚在水中溶解度不大 | |
| D. | 二氧化碳气体通入苯酚钠溶液能生成苯酚 |
10.下列物质熔化时,化学键未被破坏的是( )
| A. | 苏打 | B. | 食盐 | C. | 干冰 | D. | 金刚石 |
17.乙苯催化脱氢制苯乙烯反应: CH2CH3(g)?
CH2CH3(g)? CH=CH2(g)+H2(g)下列说法中不正确的是( )
CH=CH2(g)+H2(g)下列说法中不正确的是( )
 CH2CH3(g)?
CH2CH3(g)? CH=CH2(g)+H2(g)下列说法中不正确的是( )
CH=CH2(g)+H2(g)下列说法中不正确的是( )| A. | 乙苯的一氯代物共有3种不同结构 | |
| B. | 苯乙烯和氢气生成乙苯的反应属于加成反应 | |
| C. | 苯乙烯分子中所有原子有可能位于同一平面上 | |
| D. | 等质量的苯和苯乙烯燃烧耗氧量相同 |
14.硼有两种天然同位素${\;}_{5}^{10}$B、${\;}_{5}^{11}$B,硼元素的相对原子质量为10.8,则硼元素中${\;}_{5}^{11}$B质量分数约为( )
| A. | 20% | B. | 81.5% | C. | 18.5% | D. | 21.5% |
15.用下列装置图进行相应的实验,其中正确的是( )
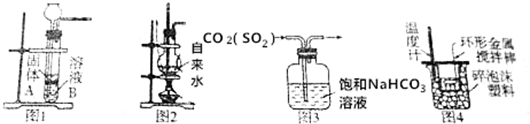

| A. | 用图1装置,若A为石灰石,B为稀硫酸,则可制取二氧化碳 | |
| B. | 用图2装置,若加上冷凝装置,可制取蒸馏水 | |
| C. | 用图3装置,可除去二氧化碳中的杂质二氧化硫 | |
| D. | 用图4装置,可测定中和热 |