题目内容
实验室用二氧化锰和浓盐酸反应制取氯气.
(1)若用200mL10mol?L-1的浓盐酸与足量的二氧化锰固体加热反应(不考虑氯化挥发),则产生氯气的物质的量为______0.5mol(填“大于”、“等于”或“小于”),原因是______.
(2)若87g二氧化锰与足量的浓盐酸反应,则被氧化的氯化氢的物质的量是多少?
解:(1)浓盐酸中含有HCl:0.2L×10mol/L═2mol
根据化学方程式:可知
在二氧化锰过量的条件下,如果HCl完全反应,会生成氯气0.5mol,但是浓盐酸与二氧化锰反应成为稀盐酸后将不会反应生成氯气,即生成的氯气会小于0.5mol,故答案为:小于;随着反应的进行,盐酸的浓度逐渐减小,稀盐酸与二氧化锰不再反应,故应小于0.5mol;
(2)n(MnO2)? ═1mol,在MnO2+4HCl?MnCl2+Cl2↑+2H2O中,每有1mol二氧化锰反应,就会有4molHCl反应,而氯元素化合价发生变化生成氯气的HCl只有2mol,据此可知:1molMnO2完全反应被氧化的氯化氢的物质的量是2mol.
═1mol,在MnO2+4HCl?MnCl2+Cl2↑+2H2O中,每有1mol二氧化锰反应,就会有4molHCl反应,而氯元素化合价发生变化生成氯气的HCl只有2mol,据此可知:1molMnO2完全反应被氧化的氯化氢的物质的量是2mol.
答:被氧化的氯化氢的物质的量是2mol.
分析:(1)根据制取氯气的反应原理分析.
(2)根据氧化还原反应和制取氯气的化学方程式分析.
点评:本题考查了实验室制取氯气的反应原理和根据化学方程式的计算,以及与制取氯气有关的氧化还原反应知识,较为综合,也较为基础,能很好地考查知识和能力.
根据化学方程式:可知
在二氧化锰过量的条件下,如果HCl完全反应,会生成氯气0.5mol,但是浓盐酸与二氧化锰反应成为稀盐酸后将不会反应生成氯气,即生成的氯气会小于0.5mol,故答案为:小于;随着反应的进行,盐酸的浓度逐渐减小,稀盐酸与二氧化锰不再反应,故应小于0.5mol;
(2)n(MnO2)?
 ═1mol,在MnO2+4HCl?MnCl2+Cl2↑+2H2O中,每有1mol二氧化锰反应,就会有4molHCl反应,而氯元素化合价发生变化生成氯气的HCl只有2mol,据此可知:1molMnO2完全反应被氧化的氯化氢的物质的量是2mol.
═1mol,在MnO2+4HCl?MnCl2+Cl2↑+2H2O中,每有1mol二氧化锰反应,就会有4molHCl反应,而氯元素化合价发生变化生成氯气的HCl只有2mol,据此可知:1molMnO2完全反应被氧化的氯化氢的物质的量是2mol.答:被氧化的氯化氢的物质的量是2mol.
分析:(1)根据制取氯气的反应原理分析.
(2)根据氧化还原反应和制取氯气的化学方程式分析.
点评:本题考查了实验室制取氯气的反应原理和根据化学方程式的计算,以及与制取氯气有关的氧化还原反应知识,较为综合,也较为基础,能很好地考查知识和能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列离子方程式书写正确的是( )
A、实验室用二氧化锰和浓盐酸制取氯气:MnO2+4HCl
| ||||
B、铜与稀硝酸反应:Cu+4H++2N
| ||||
C、向氯化铝溶液中通入过量氨气:A13++4OH-?A1
| ||||
D、向Ca(OH)2溶液中加入过量NaHCO3溶液:Ca2++2HC
|
实验室常用强氧化剂(如KMnO4、KClO3、MnO2等)氧化浓盐酸的方法来制备氯气.某研究性学习小组欲探究用Na2O2与浓盐酸制备并检验氯气.供选用的实验试剂及装置如下(部分导管、蒸馏水略):
a、Na2O2 b、浓盐酸 c、碱石灰 d、NaOH溶液 e、淀粉-KI溶液
f、CaCO3g、石蕊试液 h、饱和NaCl溶液
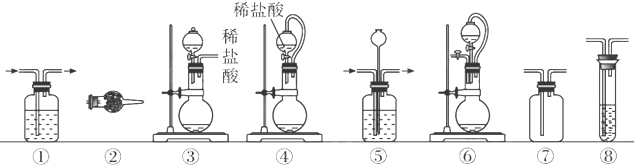
(1)写出实验室用二氧化锰和浓盐酸反应制备氯气的离子方程式
(2)写出用Na2O2与浓盐酸制备氯气的化学方程式 .该反应中盐酸的作用是
(3)下列装置组合最合理的是 (填序号,需考虑实验结束撤除装置时残留有害气体的处理).
(4)尾气经处理后仍有较多气体排出,其主要原因可用化学方程式表示为: .
(5)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:
① ,
② .
a、Na2O2 b、浓盐酸 c、碱石灰 d、NaOH溶液 e、淀粉-KI溶液
f、CaCO3g、石蕊试液 h、饱和NaCl溶液

(1)写出实验室用二氧化锰和浓盐酸反应制备氯气的离子方程式
(2)写出用Na2O2与浓盐酸制备氯气的化学方程式
(3)下列装置组合最合理的是
| 组合 | 制备装置 | 净化装置 | 检验装置/试剂 | 尾气处理装置 |
| A | ③ | ② | ⑦/e | ⑤ |
| B | ③⑥ | ① | ⑧/g | ① |
| C | ④ | ① | ⑤/e | ② |
| D | ⑥ | ⑤ | ⑧/g | ① |
(5)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:
①
②
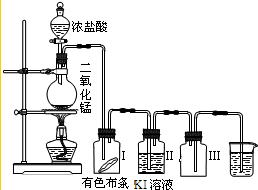 某同学实验室用下列装置探究氯气的性质.
某同学实验室用下列装置探究氯气的性质.