题目内容
将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体的体积为11.2L(标准状况),欲使铜与硝酸反应产生的气体在NaOH溶液中全部转化为NaNO3,至少需要30%的双氧水的质量为( )
| A、54g | B、57.8g |
| C、47.8g | D、33.6g |
考点:化学方程式的有关计算
专题:计算题
分析:Cu与硝酸反应得到硝酸铜与NO和NO2混合气体,NO和NO2混合气体再在双氧水、碱性条件下转化为NaNO3,纵观整个过程,根据电子转移守恒,Cu提供的电子等于过氧化氢获得的电子,据此计算过氧化氢的物质的量,再根据m=nM计算过氧化氢的质量,进而计算需要30%的双氧水的质量.
解答:
解:Cu与硝酸反应得到硝酸铜与NO和NO2混合气体,NO和NO2混合气体再在双氧水、碱性条件下转化为NaNO3,纵观整个过程,根据电子转移守恒,Cu提供的电子等于过氧化氢获得的电子,
32.64g铜的物质的量=
=0.51mol,故Cu提供电子为0.51mol×2=1.02mol,故需要过氧化氢的物质的量=
=0.51mol,过氧化氢的质量=0.51mol×34g/mol=17.34g,需要30%的双氧水的质量=
=57.8g,故选B.
32.64g铜的物质的量=
| 32.64g |
| 64g/mol |
| 1.02mol |
| 2 |
| 17.34g |
| 30% |
点评:本题考查氧化还原反应有关计算,关键是利用整体法结合守恒思想确定Cu提供的电子等于过氧化氢获得的电子,侧重考查学生分析解决问题的能力,难度中等.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
由1-氯丁烷制取1,2-二溴丁烷时,需要经过下列哪几步反应( )
| A、加成→消去 |
| B、消去→加成 |
| C、取代→加成 |
| D、消去→取代 |
下列离子方程式书写正确的是( )
| A、用双氧水和稀硫酸处理印刷电路板:Cu+H2O2+2H+=Cu2++2H2O | ||||
B、实验室制氯气:MnO2+4HCl(浓)
| ||||
| C、用FeS除去工业废水中的Hg2+:Hg2++S2-=HgS↓ | ||||
| D、向次氯酸钠溶液中通入少量二氧化硫:ClO-+SO2+H2O=Cl-+SO42-+2H+ |
 下列关于如图装置的说法正确的是( )
下列关于如图装置的说法正确的是( )| A、若断开K1关闭K2,X、Y均为石墨,Z是NaCl溶液,则X 附近能得到氢氧化钠 |
| B、若断开K1关闭K2,X是纯铜,Y是粗铜,Z是CuSO4溶液,则该装置可用于铜的精炼 |
| C、若断开K2关闭K1,X是Cu,Y是Fe,Z是含有空气的海水,则该装置可用于保护Fe |
| D、若断开K2关闭K1,X是Cu,Y是Zn,Z是稀H2SO4,则溶液中SO42-移向Y极 |
下列有关物质的性质或应用的说法不正确的是( )
| A、工业上可用铁质容器储存、运输浓硝酸或浓硫酸 |
| B、水玻璃可用于生产黏合剂和防火剂 |
| C、将SO2(或CO2)气体通入到BaCl2溶液中,可生成BaSO3(或BaCO3)沉淀 |
| D、纯净的SiO2是现代光学及光纤制品的基本原料 |
下列关于阿伏加德罗常数的说法不正确的是( )
| A、6.02×1023就是阿伏加德罗常数 |
| B、12 g 12C含有的碳原子数就是阿伏加德罗常数的数值 |
| C、含有阿伏加德罗常数个粒子的物质的量肯定是1 mol |
| D、17g NH3所含原子数约是2.408×1024 |
 如图所示,a极为Fe,b极为Cu,c、d极均为Pt,下列说法不正确的是( )
如图所示,a极为Fe,b极为Cu,c、d极均为Pt,下列说法不正确的是( )| A、甲为原电池,乙为电解池 |
| B、电子从b极流出,经导线流到c极 |
| C、b极的电极反应式为:Cu2++2e-=Cu |
| D、d极的电极反应式为:2H2O+2e-=H2↑+2OH- |
下列叙述正确的是( )
| A、Fe分别与氯气和稀盐酸反应所得氯化物相同 |
| B、铁粉中混有铝粉既可用过量的NaOH溶液,也可以用过量FeCl3充分反应过滤除去 |
| C、Li、Na、K的原子半径和密度随原子序数的增加而增大 |
| D、最外层电子数为2的元素不一定位于周期表中第二纵行 |
符合如图阴影部分的物质是( )
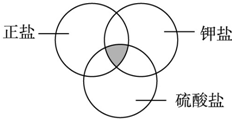

| A、KNO3 |
| B、KHSO4 |
| C、K2S |
| D、K2SO4 |