题目内容
下列有关物质的性质或应用的说法不正确的是( )
| A、工业上可用铁质容器储存、运输浓硝酸或浓硫酸 |
| B、水玻璃可用于生产黏合剂和防火剂 |
| C、将SO2(或CO2)气体通入到BaCl2溶液中,可生成BaSO3(或BaCO3)沉淀 |
| D、纯净的SiO2是现代光学及光纤制品的基本原料 |
考点:铁的化学性质,二氧化硫的化学性质,硅和二氧化硅,含硅矿物及材料的应用
专题:元素及其化合物
分析:A、铁在常温下在浓硫酸、浓硝酸中发生钝化阻止反应进行;
B、水玻璃是硅酸钠的水溶液是一种矿物胶和防火剂;
C、二氧化硫、二氧化碳气体通入氯化钡溶液不能发生反应;
D、二氧化硅是光导纤维的主要成分;
B、水玻璃是硅酸钠的水溶液是一种矿物胶和防火剂;
C、二氧化硫、二氧化碳气体通入氯化钡溶液不能发生反应;
D、二氧化硅是光导纤维的主要成分;
解答:
解:A、铁在常温下在浓硫酸、浓硝酸中发生钝化阻止反应进行,工业上可用铁质容器储存、运输浓硝酸或浓硫酸,故A正确;
B、水玻璃是硅酸钠的水溶液是一种矿物胶和防火剂,水玻璃可用于生产黏合剂和防火剂,故B正确;
C、二氧化硫、二氧化碳气体通入氯化钡溶液不能发生反应,不能生成沉淀,故C错误;
D、二氧化硅是光导纤维的主要成分,纯净的SiO2是现代光学及光纤制品的基本原料,故D正确;
故选C.
B、水玻璃是硅酸钠的水溶液是一种矿物胶和防火剂,水玻璃可用于生产黏合剂和防火剂,故B正确;
C、二氧化硫、二氧化碳气体通入氯化钡溶液不能发生反应,不能生成沉淀,故C错误;
D、二氧化硅是光导纤维的主要成分,纯净的SiO2是现代光学及光纤制品的基本原料,故D正确;
故选C.
点评:本题考查了铁、二氧化硫、二氧化硅及其化合物性质的分析判断,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
下列说法错误的是( )
A、 用图装置可以收集HCl、SO2等气体 |
| B、用移液管取液后,将移液管垂直放入稍倾斜的容器中,管尖与容器内壁不能接触,松开食指使溶液全部流出 |
| C、用含氟牙膏刷牙,使牙齿更加坚固,是因为Ca10(PO4F)6F2比Ca10(PO4)6(OH)2更难溶 |
| D、在“镀锌铁皮锌镀层厚度的测定”实验中,当反应速率突然减小时,立即取出铁皮用蒸馏水洗净,再在酒精灯火焰上灼烧,将导致实验结果偏低 |
下列说法符合事实的是( )
| A、常温下由水电离产生的c(H+)=10-12mol/L的溶液中加入铝粉都能够产生氢气 |
| B、已知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12.在含Cl-、CrO42-浓度相同的溶液中滴加几滴稀AgNO3溶液时,则先生成AgCl沉淀 |
| C、电解硫酸铜溶液一段时间后,加入氧化铜固体不可能使溶液恢复到原来的浓度 |
| D、在NaAlO2和Na2CO3的混合溶液中逐滴滴加盐酸直至过量,开始没有沉淀,随后产生沉淀,最后沉淀消失 |
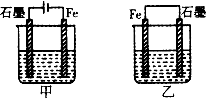 如图所示装置,均盛有等体积等浓度的稀硫酸,工作相同的时间后测得均通过n mol e-.下列叙述错误的是(不考虑溶液体积的变化)( )
如图所示装置,均盛有等体积等浓度的稀硫酸,工作相同的时间后测得均通过n mol e-.下列叙述错误的是(不考虑溶液体积的变化)( )| A、铁棒的腐蚀程度:甲<乙 |
| B、碳电极上发生反应的电极反应式相同 |
| C、溶液的pH:甲减小,乙增大 |
| D、甲乙产生气体的体积(相同条件)比为3:2 |
将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体的体积为11.2L(标准状况),欲使铜与硝酸反应产生的气体在NaOH溶液中全部转化为NaNO3,至少需要30%的双氧水的质量为( )
| A、54g | B、57.8g |
| C、47.8g | D、33.6g |
下列各类关系中能说明反应 N2+3H2?2NH3 已达到平衡状态的是( )
| A、3V正(N2)=V逆(H2) |
| B、V正(N2)=V逆(NH3) |
| C、2V正(H2)=3V正(NH3) |
| D、V正(N2)=3V逆(H2) |
下列叙述不正确的是( )
| A、手机上用的锂离子电池属于二次电池 |
| B、钢铁吸氧腐蚀的正极反应:4OH--4e-=2H2O+O2↑ |
| C、中和热与化学反应方程式的计量数无关 |
| D、所有反应物的键能之和小于所有生成物的键能之和的反应为放热反应 |
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、标准状况下,33.6L HF中含有氟原子的数目为1.5NA |
| B、常温常压下,9.2g二氧化氮和四氧化二氮的混合物含有氮原子的数目为0.2NA |
| C、50mL18.4mol?L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA |
| D、0.1mol铁溶于足量氯水中,转移电子的总数为0.2NA |