题目内容
有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如图所示的装置进行实验.通入SO2气体,将带余烬的木条插入试管C中,木条复燃.
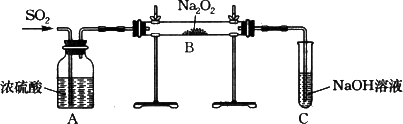
请回答下列问题:
(1)第1小组同学认为Na2O2与SO2反应生成了Na2SO3和O2,该反应的化学方程式是________.
(2)请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3.
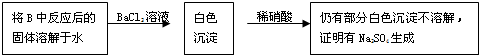
(3)第2小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成.为检验是否有Na2SO4生成,他们设计了如下方案:

上述方案是否合理?________.请简要说明两点理由:①________,②________.
答案:
解析:
解析:
|
答案:(1)2Na2O2+2SO2=2Na2SO3+O2. (2)取白色固体,加稀硫酸,产生能使品红溶液褪色的气体. (3)不合理;①稀硝酸能将亚硫酸钡氧化为硫酸钡;②如果反应后的固体中还残留Na2O2,它溶于水后能将亚硫酸根氧化成硫酸根. 解析:SO2与Na2O2反应原理不同于CO2与Na2O2反应原理,因SO2有较强的还原性,能被强氧化剂Na2O2氧化成Na2SO4,结合O2、 评注:本题属于综合实验题,此类试题的考查趋向为:一是小巧灵活型的方向是发展方向;二是以气体为核心仍是考查的方向;三是探究性实验与研究性学习的整合是未来的特色. |

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
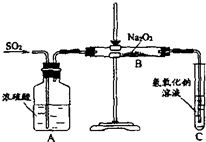


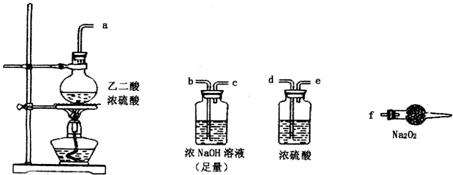
 有两个实验小组的同学探究一氧化碳、二氧化硫与过氧化钠的反应.请回答下列问题:
有两个实验小组的同学探究一氧化碳、二氧化硫与过氧化钠的反应.请回答下列问题:

 0
0