题目内容
7.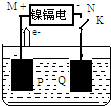 镍镉电池是一种十分常见的二次电池,它具有成本低、性能好的优点.该电池充、放电时的反应为:Cd+2NiOOH+2H2O$?_{充电}^{放电}$Cd(OH)2+2Ni(OH)2.如图用该电池电解AgNO3溶液,M、N是代表电池的两极,P、Q表示两惰性电极,Cd的相对原子质量为112,则下列有关说法不正确的是( )
镍镉电池是一种十分常见的二次电池,它具有成本低、性能好的优点.该电池充、放电时的反应为:Cd+2NiOOH+2H2O$?_{充电}^{放电}$Cd(OH)2+2Ni(OH)2.如图用该电池电解AgNO3溶液,M、N是代表电池的两极,P、Q表示两惰性电极,Cd的相对原子质量为112,则下列有关说法不正确的是( )| A. | N是镍镉电池的负极,其电极反应为Cd+2OH--2e-=Cd(OH)2 | |
| B. | 当N极有11.2gCd溶解时,P极放出气体2.24L | |
| C. | K闭合后的短时间内,N极区溶液的pH变小 | |
| D. | Q是电解池的阴极,其电极反应为Ag++e-=Ag |
分析 放电时Cd为负极,电极反应式为Cd-2e-+2OH-=Cd(OH)2,正极反应式为NiOOH+H2O+e-═Ni(OH)2+OH-,用惰性电极电解AgNO3溶液,发生4AgNO3+2H2O$\frac{\underline{\;电解\;}}{\;}$4Ag+O2↑+4HNO3,以此来解答.
解答 解:A.由图示可知N为原电池的负极,发生氧化反应,电极方程式为Cd+2OH--2e-=Cd(OH)2,故A正确;
B.负极电极反应式为Cd-2e-+2OH-=Cd(OH)2,当N极有11.2gCd溶解时,转移0.2mol电子,P极生成氧气,由于不确定气体存在的条件,则不能确定体积,故B错误;
C.K闭合后的短时间内,N极区发生4OH--4e-=2H2O+O2↑,溶液的pH变小,故C正确;
D.Q是电解池的阴极,发生含有反应,析出银,其电极反应为Ag++e-=Ag,故D正确.
故选B.
点评 本题综合考查原电池、电解池知识,为高频考点,根据元素化合价变化确定正负极、阴阳极发生的反应,难点是书写电极反应式,知道正负极与阳极、阴极电极反应式的关系,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列有关说法中,正确的是( )
| A. | 生铁、不锈钢、青铜都属于合金 | |
| B. | 14C可用于文物年代的鉴定,14C与12C互为同素异形体 | |
| C. | 食醋、纯碱、食盐分别属于酸、碱、盐 | |
| D. | 糖类、油脂和蛋白质都是天然高分子化合物 |
18.要使蛋白质从溶液中析出面又不改变蛋白质的性质,应加入的试剂是( )
| A. | 乙醇 | B. | 福尔马林 | C. | 乙酸铅浓溶液 | D. | (NH4)2S04浓溶液 |
15.下列有关Na2O2的说法正确的是( )
| A. | Na2O2中阴阳离子个数比为1:1 | |
| B. | Na2O2是一种白色固体 | |
| C. | Na2O2可用于呼吸面具中提供氧气 | |
| D. | Na2O2的漂白原理与SO2的漂白原理完全相同 |
2.在氯化镁和氯化铝的混合液中,Mg2+的物质的量为0.04mol,Al3+的物质的量为0.06mol.要使Mg2+全部转化为沉淀而分离出来,至少需要加入4mol/L NaOH溶液的体积为( )
| A. | 40mL | B. | 72mL | C. | 80mL | D. | 128mL |
12.下列有关实验操作和现象描述的对应关系正确的是( )
| A. | 向蔗糖中加入浓硫酸,蔗糖变黑,并放出无色无味气体 | |
| B. | 将NaOH溶液逐滴滴入FeSO4溶液中,只观察到白色沉淀 | |
| C. | 向AlCl3溶液中逐滴加入氨水至过量,产生白色沉淀 | |
| D. | 将砂纸打磨过的铝箔加热至熔化,熔化的铝以小液滴的形式滴落下来 |
19.三位科学家保罗•克拉兹等因在氟利昂和臭氧层方面的工作获得诺贝尔化学奖,他们的研究揭示了大气中臭氧层被破坏的机理,如图所示.下列说法不正确的是( )

| A. | 氯原子在反应中做催化剂 | |
| B. | 过氧化氯的结构式为:O-Cl-Cl-O | |
| C. | 臭氧分子最终转变成氧气分子 | |
| D. | 过程②中一氧化氯断键形成过氧化氯 |
16.取10ml盐酸注入25ml酸式滴定管中,则液面读数( )
| A. | 大于15mL | B. | 小于10mL | ||
| C. | 恰好在15mL处 | D. | 在10mL到15mL之间 |
下列实验操作完全正确的是 ( )
编号 | 实验 | 操作 |
A | 用浓硫酸配制一定浓度的稀硫酸 | 准确量取浓硫酸,将浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中。 |
B | 除去BaSO4中的少量BaCO3 | 加入足量盐酸,充分反应后,过滤、洗涤、干燥 |
C | 量取盐酸溶液 | 用25 mL量筒量取4.0 mol/L的盐酸5.62 mL |
D | 取出分液漏斗中所需的上层液体 | 下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 |