题目内容
16.取10ml盐酸注入25ml酸式滴定管中,则液面读数( )| A. | 大于15mL | B. | 小于10mL | ||
| C. | 恰好在15mL处 | D. | 在10mL到15mL之间 |
分析 滴定管中小刻度在上方、大刻度在下方,且滴定管中最大看到下方还能储存部分液体,据此分析解答.
解答 解:滴定管中小刻度在上方、大刻度在下方,且滴定管中最大看到下方还能储存部分液体,所以用移液管取10mL烧碱溶液注入25mL洁净的碱式滴定管中,其读数大于15mL,即在15mL下面刻度处,
故选A.
点评 本题考查滴定管,明确滴定管中刻度值大小顺序是解本题关键,注意滴定管最大刻度处还能贮存液体,为易错点,知道酸碱式滴定管的区别,题目难度不大.

练习册系列答案
相关题目
7.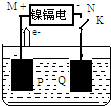 镍镉电池是一种十分常见的二次电池,它具有成本低、性能好的优点.该电池充、放电时的反应为:Cd+2NiOOH+2H2O$?_{充电}^{放电}$Cd(OH)2+2Ni(OH)2.如图用该电池电解AgNO3溶液,M、N是代表电池的两极,P、Q表示两惰性电极,Cd的相对原子质量为112,则下列有关说法不正确的是( )
镍镉电池是一种十分常见的二次电池,它具有成本低、性能好的优点.该电池充、放电时的反应为:Cd+2NiOOH+2H2O$?_{充电}^{放电}$Cd(OH)2+2Ni(OH)2.如图用该电池电解AgNO3溶液,M、N是代表电池的两极,P、Q表示两惰性电极,Cd的相对原子质量为112,则下列有关说法不正确的是( )
 镍镉电池是一种十分常见的二次电池,它具有成本低、性能好的优点.该电池充、放电时的反应为:Cd+2NiOOH+2H2O$?_{充电}^{放电}$Cd(OH)2+2Ni(OH)2.如图用该电池电解AgNO3溶液,M、N是代表电池的两极,P、Q表示两惰性电极,Cd的相对原子质量为112,则下列有关说法不正确的是( )
镍镉电池是一种十分常见的二次电池,它具有成本低、性能好的优点.该电池充、放电时的反应为:Cd+2NiOOH+2H2O$?_{充电}^{放电}$Cd(OH)2+2Ni(OH)2.如图用该电池电解AgNO3溶液,M、N是代表电池的两极,P、Q表示两惰性电极,Cd的相对原子质量为112,则下列有关说法不正确的是( )| A. | N是镍镉电池的负极,其电极反应为Cd+2OH--2e-=Cd(OH)2 | |
| B. | 当N极有11.2gCd溶解时,P极放出气体2.24L | |
| C. | K闭合后的短时间内,N极区溶液的pH变小 | |
| D. | Q是电解池的阴极,其电极反应为Ag++e-=Ag |
11.25℃时,下列有关溶液中各微粒的物质的量浓度关系正确的是( )
| A. | 0.1mol/L的NH4Cl溶液:c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| B. | 0.1mol/L的CH3COOH溶液:c(CH3COOH)>c(H+)>c(CH3COO-)>c(OH-) | |
| C. | pH=4的FeCl3溶液:c(Cl-)>c(H+)>c(Fe3+)>c(OH-) | |
| D. | pH=11的CH3COONa溶液:c(Na+)+c(H+)=c(CH3COO-)+c(CH3COOH) |
7.几种短周期元素的原子半径及主要化合价如下表所示:
下列说法中正确的是( )
| 元素符号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5,+3,-3 | -2 |
| A. | 一定条件下,Z的单质与W的常见单质直接生成ZW2 | |
| B. | Z最高价氧化物对应水化物与其氢化物能发生化合反应生成离子化合物 | |
| C. | Y的最高价氧化物对应水化物溶于氨水 | |
| D. | 相同条件下,X,Y的单质分别与盐酸反应时,后者反应剧烈些 |




 3C(g)+D(g)达到平衡时,C的浓度为Wmol/L,若维持容器体积和温度不变,按下列四种方法改变起始物质,达到平衡后,C的浓度仍为Wmol/L的是( )
3C(g)+D(g)达到平衡时,C的浓度为Wmol/L,若维持容器体积和温度不变,按下列四种方法改变起始物质,达到平衡后,C的浓度仍为Wmol/L的是( ) 2C(g)+D(g),在不同条件下的反应速率如下,其中反应速率最快的是( )
2C(g)+D(g),在不同条件下的反应速率如下,其中反应速率最快的是( ) v(C)=0.8 mol/(L•min) D.v(D)=0.01mol/(L•s)
v(C)=0.8 mol/(L•min) D.v(D)=0.01mol/(L•s)