题目内容
15.设NA表示阿伏加德罗常数,下列叙述中正确的是( )| A. | 1.8 g 的NH4+中含有的电子数为NA | |
| B. | 11.2L氯气与钠反应完全转化为氯化钠时得到的电子数为NA | |
| C. | 常温常压下,48gO3含有的氧原子数为NA | |
| D. | 标况下,11.2 L四氯化碳所含的分子数为0.5NA |
分析 A、求出铵根离子的物质的量,然后根据1mol铵根离子中含10mol电子来分析;
B、氯气所处的状态不明确;
C、臭氧由氧原子构成;
D、标况下四氯化碳为液态.
解答 解:A、1.8g铵根离子的物质的量为0.1mol,而1mol铵根离子中含10mol电子,故0.1mol铵根离子中含NA个电子,故A正确;
B、氯气所处的状态不明确,故其物质的量无法计算,则转化为氯化钠时得到的电子数无法计算,故B错误;
C、臭氧由氧原子构成,故48g臭氧中含有的氧原子的物质的量为n=$\frac{48g}{16g/mol}$=3mol,故为3NA个,故C错误;
D、标况下四氯化碳为液态,故不能根据气体摩尔体积来计算其物质的量和含有的分子个数,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
5.利用如图装置能制取并收集到相应气体的是( )
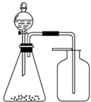

| A. | 浓氨水与固体CaO制氨气 | B. | 盐酸与CaCO3固体制CO2 | ||
| C. | 稀硝酸与铜片制NO | D. | 饱和食盐水与电石制乙炔 |
6. 如图所示的原电池装置,X、Y为两电极,电解质溶液为硫酸铜,外电路中的电子流向如图所示,对此装置的下列说法正确的是( )
如图所示的原电池装置,X、Y为两电极,电解质溶液为硫酸铜,外电路中的电子流向如图所示,对此装置的下列说法正确的是( )
 如图所示的原电池装置,X、Y为两电极,电解质溶液为硫酸铜,外电路中的电子流向如图所示,对此装置的下列说法正确的是( )
如图所示的原电池装置,X、Y为两电极,电解质溶液为硫酸铜,外电路中的电子流向如图所示,对此装置的下列说法正确的是( )| A. | X极上发生的是还原反应,Y极上发生的是氧化反应 | |
| B. | 外电路的电流方向为:X→外电路→Y | |
| C. | 若两电极都是金属,则它们的活动性为X<Y | |
| D. | 若两电极分别为Zn和石墨棒,则Y极质量增重 |
10.苹果酸的结构简式为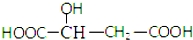 ,下列说法正确的是( )
,下列说法正确的是( )
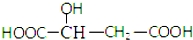 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 苹果酸中能发生酯化反应的官能团有2种 | |
| B. | 1mol苹果酸可与3mol NaOH发生中和反应 | |
| C. | 1mol苹果酸与足量金属Na反应生成1mol H2 | |
| D. | 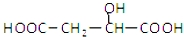 与苹果酸互为同分异构体 与苹果酸互为同分异构体 |
20.某澄清透明的溶液中,下列离子组可以大量共存的是( )
| A. | H+、Na+、SO42-、Cu2+ | B. | Ba2+、Mg2+、Cl-、SO42- | ||
| C. | H+、K+、OH-、NO3- | D. | NO3-、I-、H+、Mg2+ |
4.已知1~18号元素的离子aW2+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )
| A. | 质子数:c>d | B. | 碱性:XOH>W(OH)2 | ||
| C. | 氢化物稳定性:H2Y>HZ | D. | 原子半径:X<W |
5.同周期元素(除稀有气体外)随核电荷数的增加,元素性质递变规律不正确的是( )
| A. | 元素的金属性减弱 | B. | 元素的非金属性增强 | ||
| C. | 单质得电子能力依次减弱 | D. | 原子半径依次减小 |
 ,写出B与浓硝酸反应的化学方程式
,写出B与浓硝酸反应的化学方程式 ,写出B与液溴反应的方程式
,写出B与液溴反应的方程式 .
.