题目内容
4.已知1~18号元素的离子aW2+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )| A. | 质子数:c>d | B. | 碱性:XOH>W(OH)2 | ||
| C. | 氢化物稳定性:H2Y>HZ | D. | 原子半径:X<W |
分析 元素周期表前三周期元素的离子aW2+、bX+、cY2-、dZ-具有相同电子层结构,核外电子数相等,所以a-2=b-1=c+2=d+1,Y、Z为非金属,应处于第二周期,故Y为O元素,Z为F元素,W、X为金属应处于第三周期,W为Mg元素,X为Na元素,以此解答该题.
解答 解:元素周期表前三周期元素的离子aW2+、bX+、cY2-、dZ-具有相同电子层结构,核外电子数相等,所以a-2=b-1=c+2=d+1,Y、Z为非金属,应处于第二周期,故Y为O元素,Z为F元素,W、X为金属应处于第三周期,W为Mg元素,X为Na元素,
A.离子的电子层结构相同,则c+2=d+1,则质子数d>c,故A错误;
B.W为Mg元素,X为Na元素,金属性W<X,金属性越强其最高价氧化物的水化物的碱性越强,所以碱性:XOH>W(OH)2,故B正确;
C.非金属性越强,其氢化物的稳定性越强,非金属性Y<Z,则氢化物的稳定性H2Y<HZ,故C错误;
D.W是Mg元素、X是Na元素,同一周期元素,原子半径随着原子序数增大而减小,所以原子半径W<X,故D错误;
故选B.
点评 本题考查原子结构和元素性质,为高频考点,正确判断元素是解本题关键,熟练掌握同一周期、同一主族元素原子结构、元素性质递变规律,题目难度不大.

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
15.设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 1.8 g 的NH4+中含有的电子数为NA | |
| B. | 11.2L氯气与钠反应完全转化为氯化钠时得到的电子数为NA | |
| C. | 常温常压下,48gO3含有的氧原子数为NA | |
| D. | 标况下,11.2 L四氯化碳所含的分子数为0.5NA |
19.利用下列实验装置进行的相应实验,不能达到实验目的是( )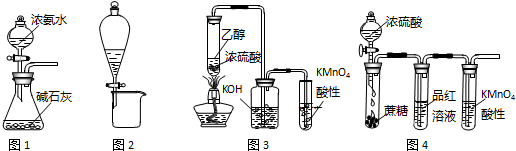

| A. | 图1装置可制取氨气 | |
| B. | 图2装置可分离CH3COONa和CH3COOC2H5混合液 | |
| C. | 图3所示装置可制取乙烯并验证其易被氧化 | |
| D. | 图4所示装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性 |
9.某烃X完全燃烧时,生成的n(H2O)=n(CO2),X不能使溴水褪色.X的分子式可能是( )
| A. | C2H2 | B. | C2H4 | C. | C3H4 | D. | C3H6 |
16.我国药学家屠呦呦作为抗疟新药青蒿素的第一发明人荣获2015年诺贝尔生理学或医学奖.青蒿素和双氢青蒿素的结构简式如图所示,下列说法错误的是( )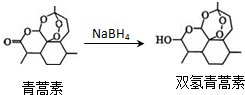

| A. | 青蒿素易溶于苯,难溶于水 | |
| B. | 由青蒿素制备双氢青蒿素的反应属于 还原反应 | |
| C. | 青蒿素可与NaOH溶液在一定条件下发生水解反应 | |
| D. | 双氢青蒿素的同分异构体不可能有芳香族化合物 |
13.下列有机物不能发生银镜反应的是( )
| A. | 葡萄糖 | B. | 甲酸乙酯 | C. | 乙酸甲酯 | D. | 甲酸 |
14.用NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 标准状况下,11.2L水所含分子数为0.5NA | |
| B. | 常温常压下,22.4L氦气中所含原子数为NA | |
| C. | 常温常压下,48gO2与O3混合气体中所含原子数为3NA | |
| D. | 0.5mol/LFe2(SO4)3溶液中,SO42-的数目为1.5NA |