题目内容
工业上电解饱和食盐水可产生氯气,氯气与石灰乳反应可制得漂白粉.若欲制得标准状况112L氯气,则求理论上消耗多少克食盐?用这些氯气理论上可生产漂白粉多少克?
考点:化学方程式的有关计算
专题:
分析:电解饱和食盐水发生的反应为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑、氯气与石灰乳反应为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,漂白粉的主要成分为CaCl2、Ca(ClO)2,将氯气的物质的量代入计算即可.
| ||
解答:
解:欲制得标准状况112L氯气,n(Cl2)=
=5mol,
由2NaCl+2H2O
2NaOH+H2↑+Cl2↑可知,消耗NaCl为5mol×2=10mol,其质量为10mol×58.5g/mol=585g;
由2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O可知,得到2.5molCaCl2、2.5molCa(ClO)2,漂白粉的质量为2.5mol×(111g/mol+143g/mol)=635g,
答:理论上消耗585克食盐,用这些氯气理论上可生产漂白粉635克.
| 112L |
| 22.4L/mol |
由2NaCl+2H2O
| ||
由2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O可知,得到2.5molCaCl2、2.5molCa(ClO)2,漂白粉的质量为2.5mol×(111g/mol+143g/mol)=635g,
答:理论上消耗585克食盐,用这些氯气理论上可生产漂白粉635克.
点评:本题考查化学反应方程式的计算,为高频考点,把握发生的化学反应及物质的量的关系为解答的关键,侧重分析能力及计算能力的考查,注意漂白粉的成分,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列有关金属及化合物用途说法中,不正确的是( )
| A、钠钾合金可用于快中子反应堆作热交换剂 |
| B、镁燃烧发出耀眼的白光,常用于制造信号弹和焰火 |
| C、铜化学性质不活泼,故古代用作铸币材料 |
| D、铝和Fe2O3混合物在常温下会发生剧烈反应,可以用于野外焊接钢轨 |
化学与生产、生活密切相关.下列有关叙述正确的是( )
| A、大气雾霾污染现象的产生与汽车尾气排放有关 |
| B、玻璃和氮化硅陶瓷都属于新型无机非金属材料 |
| C、空气中的臭氧对人体健康有益无害 |
| D、活性炭与二氧化硫都可用于漂白,其漂白原理相同 |


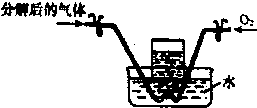 已知Fe(NO3)2受热分解产物为金属氧化物、NO2、O2.某兴趣小组同学对固体产物中Fe的化合物进行了如下探究:
已知Fe(NO3)2受热分解产物为金属氧化物、NO2、O2.某兴趣小组同学对固体产物中Fe的化合物进行了如下探究:
