题目内容
下列有关物质的性质及应用说法正确的是( )
| A、Si具有导电性,可用作半导体材料 |
| B、难熔的Al2O3制成的坩埚,可用于熔融烧碱 |
| C、氯气具有酸性,可与烧碱或石灰乳反应制备含氯消毒剂 |
| D、Cl2和SO2均有漂白性,均可使含有酚酞的NaOH溶液褪色 |
考点:硅和二氧化硅,氯气的化学性质,二氧化硫的化学性质,镁、铝的重要化合物
专题:元素及其化合物
分析:A.Si导电性介于导体和绝缘体之间,可用用作半导体材料;
B.氧化铝与烧碱反应;
C.氯气与烧碱或石灰乳反应体现了氯气的氧化性和还原性;
D.次氯酸的漂白性是利用次氯酸的强氧化性,二氧化硫的漂白性是利用二氧化硫和有色物质生成无色物质;
B.氧化铝与烧碱反应;
C.氯气与烧碱或石灰乳反应体现了氯气的氧化性和还原性;
D.次氯酸的漂白性是利用次氯酸的强氧化性,二氧化硫的漂白性是利用二氧化硫和有色物质生成无色物质;
解答:
解:A.Si导电性介于导体和绝缘体之间,可用作半导体材料,故A正确;
B.氧化铝与烧碱反应,则不能利用Al2O3制成的坩埚熔融烧碱,故B错误;
C.氯气与烧碱或石灰乳反应体现了氯气的氧化性和还原性,不是酸性,故C错误;
D.氯气无漂白性,与水反应生成次氯酸,次氯酸具有强氧化性,具有漂白性,可使含有酚酞的NaOH溶液褪色;二氧化硫的漂白性是利用二氧化硫和有色物质生成无色物质,二氧化硫能与氢氧化钠反应,从而使溶液褪色,不能体现SO2的漂白性,故D错误;
故选A.
B.氧化铝与烧碱反应,则不能利用Al2O3制成的坩埚熔融烧碱,故B错误;
C.氯气与烧碱或石灰乳反应体现了氯气的氧化性和还原性,不是酸性,故C错误;
D.氯气无漂白性,与水反应生成次氯酸,次氯酸具有强氧化性,具有漂白性,可使含有酚酞的NaOH溶液褪色;二氧化硫的漂白性是利用二氧化硫和有色物质生成无色物质,二氧化硫能与氢氧化钠反应,从而使溶液褪色,不能体现SO2的漂白性,故D错误;
故选A.
点评:本题考查物质的性质,为高频考点,综合考查元素化合物知识,把握物质的性质及发生的反应为解答的关键,注意物质的性质与用途的关系,题目难度中等.

练习册系列答案
相关题目
下列有关工业生产过程的叙述正确的是( )
| A、合成氨工业中及时将NH3液化分离,可加快反应速率,并提高N2、H2的转化率 |
| B、向汽油中添加甲醇后,该混合燃料的热值不变 |
| C、氯碱工业中采用阴离子交换膜法,可防止阴极产生的Cl2和阳极产生的碱反应 |
| D、目前淡化海水的方法有多种,其中蒸馏法历时最久,成本最高 |
检验某未知溶液中是否含有SO42-,下列操作最合理的是( )
| A、先加稀硝酸酸化,再加入Ba(NO3)2溶液 |
| B、加BaCl2溶液即可 |
| C、先加盐酸酸化,再加BaCl2溶液 |
| D、加Ba(NO3)2溶液即可 |
室温下,0.1mol/L氨水10mL,加蒸馏水稀释到1L后,下列变化中正确的是 ①电离度增大 ②C(OH-)增大 ③C(H+]增大 ④KW 增大⑤导电性增强 ⑥
增大( )
| c(OH-) |
| c(NH3?H2O) |
| A、①②③ | B、①③⑤ |
| C、①③⑥ | D、②④⑥ |
人类的生活离不开材料,
①塑料广泛应用与生产、生活的各个领域,聚乙烯塑料属于 (填序号)
A.有机高分子材料 B.无机非金属材料 C.金属材料
②蚕丝、尼龙、棉花这三种常见的纤维中,主要成分为蛋白质的是 .
①塑料广泛应用与生产、生活的各个领域,聚乙烯塑料属于
A.有机高分子材料 B.无机非金属材料 C.金属材料
②蚕丝、尼龙、棉花这三种常见的纤维中,主要成分为蛋白质的是
下列有关氯水的叙述,正确的是( )
| A、新制氯水可使无色酚酞试纸先变红,后褪色 |
| B、新制的氯水只含Cl2和H2O分子 |
| C、氯水放置数天后,酸性增强 |
| D、光照氯水有气泡逸出,该气体是Cl2 |
下列反应的离子方程式书写中,正确的是( )
| A、稀硫酸与铁粉反应:2Fe+6H+=2Fe3++3H2↑ |
| B、氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu |
| C、碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
| D、氢氧化钡溶液与稀硫酸反应:Ba2++SO42-=BaSO4↓ |
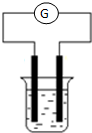 现有A、B、C、D和Cu五种金属片,将其分别用导线连接后浸入稀硫酸中(如图),每次实验时,通过灵敏电流计测出电子流动方向如下:
现有A、B、C、D和Cu五种金属片,将其分别用导线连接后浸入稀硫酸中(如图),每次实验时,通过灵敏电流计测出电子流动方向如下: