题目内容
7.下列反应符合该卡通情境的是( )
| A. | C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ | B. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | ||
| C. | Cu+2AgNO3═Cu(NO3)2+2Ag | D. | BaCl2+Na2SO4═BaSO4↓+2NaCl |
分析 由图可知,发生金属单质之间的置换反应,较活泼金属置换出较不活泼金属,以此来解答.
解答 解:由图可知,发生金属单质之间的置换反应,较活泼金属置换出较不活泼金属,只有C为金属单质之间的置换反应,A中C为非金属,B不是置换反应,D为复分解反应,
故选C.
点评 本题考查金属单质之间的置换反应,为高频考点,把握金属活泼性及应用为解答的关键,侧重分析与应用能力的考查,注意金属活动性顺序表的应用,题目难度不大.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案
相关题目
17.如表是元素周期表的一部分,用化学用语回答:
(1)②的元素符号为F.
(2)比较元素③和⑦的原子半径大小:③<⑦(填“>”或“<”).
(3)绘出元素⑤的离子结构示意图 .
.
(4)元素①的氢化物的电子式为 ,将该氢化物通入④和⑥形成的化合物的水溶液中,发生反应的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
,将该氢化物通入④和⑥形成的化合物的水溶液中,发生反应的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 二 | ] | ① | ② | ||||
| 三 | ③ | ④ | ⑤ | ⑥ | |||
| 四 | ⑦ |
(2)比较元素③和⑦的原子半径大小:③<⑦(填“>”或“<”).
(3)绘出元素⑤的离子结构示意图
 .
.(4)元素①的氢化物的电子式为
 ,将该氢化物通入④和⑥形成的化合物的水溶液中,发生反应的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
,将该氢化物通入④和⑥形成的化合物的水溶液中,发生反应的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
18.原子序数依次增大的短周期元素a、b、c、d,它们的最外层电子数分别依次为6、7、1、3.a、b、c、d形成的简单离子与氖原子电子层结构相同.下列叙述错误的是( )
| A. | d的最高价氧化物对应水化物可溶于c的最高价氧化物对应的水化物的溶液 | |
| B. | a和c形成的离子化合物中可能含有共价键 | |
| C. | 四种元素离子半径:c>d>a>b | |
| D. | c是短周期元素中金属性最强的元素,b是短周期元素中非金属性最强的元素 |
15.下列关于实验的说法错误的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 检验CO2与NaOH溶液反应后 的溶液中是否有Na2CO3 | 取少量反应后的溶液,滴加BaC12溶液,看是否有沉淀生成 |
| B | 除去甲烷中含有的乙烯杂质 | 将气体通入到酸性高锰酸钾溶液后,再通过装有碱石灰的干燥管 |
| C | 证明酸性:H2CO3>H3BO3 | 向Na2CO3中滴入过量H3BO3溶液,无气泡冒出 |
| D | 分离Fe(OH)3胶体和FeCl3溶液 | 将混合液倒入过滤器中过滤 |
| A. | A | B. | B | C. | C | D. | D |
12.下列说法不正确的是( )
| A. | 麦芽糖及其水解产物均能发生银镜反应 | |
| B. | 用溴水即可鉴别苯酚溶液、2,4-己二烯和甲苯 | |
| C. | 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH | |
| D. | 用甘氨酸( 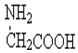 )和丙氨酸( )和丙氨酸( 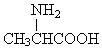 )缩合最多可形成4种二肽(不考虑形成环状) )缩合最多可形成4种二肽(不考虑形成环状) |
19.已知2SO2(g)+O2(g)?2SO3(g)为放热反应,对该反应的下列说法正确的是( )
| A. | 1mol O2的能量一定高于2mol SO2的能量 | |
| B. | 1mol SO2的能量一定高于1mol SO3的能量 | |
| C. | 因为该反应是放热反应,所以不必加热就可以发生 | |
| D. | 2mol SO3的能量一定低于2mol SO2和1mol O2的总能量 |
16.日本福岛核泄露事故的铯-137其符号表示为${\;}_{55}^{137}$Cs,下列关于该原子的说法不正确的是( )
| A. | 质子数为137 | B. | 质子数为55 | ||
| C. | 电子数为82 | D. | 中子数与质子数之差为27 |
17.当干冰气化时,下列所述中发生变化的是( )
| A. | 分子大小 | B. | 范德华力 | C. | 分子内共价键 | D. | 化学性质 |
