题目内容
短周期元素的离子W2+、X+、Y2-、Z-都具有相同的电子层结构,下列推断正确的是( )
| A、原子半径:W>X>Z>Y |
| B、热稳定性:H2Y>HZ |
| C、离子半径:W2+>Y2- |
| D、碱性:XOH>W(OH)2 |
考点:原子结构与元素周期律的关系
专题:
分析:根据W2+、X+、Y2-、Z-四种离子具有相同的电子层结构,依据“阴上阳下”规律(具有相同的核外电子排布的微粒,阴离子在上一周期,阳离子在下一周期)和离子带电荷数,可以推测其对应原子在周期表中的位置关系,如下图所示: ,然后根据元素周期律推断物质的性质,微粒半径大小比较.
,然后根据元素周期律推断物质的性质,微粒半径大小比较.
 ,然后根据元素周期律推断物质的性质,微粒半径大小比较.
,然后根据元素周期律推断物质的性质,微粒半径大小比较.解答:
解:对应原子在周期表中的位置关系,如下图所示: ,
,
A.X W电子层数比Y Z多,半径大,再根据同周期原子半径依次减小规律,推出半径大小顺序:X>W>Y>Z,故A错误;
B.同周期非金属性依次增强,故氢化物稳定性依次增强,热稳定性:H2Y<HZ,故B错误;
C.根据“阴上阳下,径小序大”规律:Y2->W2+,故C错误;
D.同周期元素金属性依次减弱,最高价氧化物对应水化物的碱性依次减弱,碱性:XOH>W(OH)2 ,故D正确.
故选D.
 ,
,A.X W电子层数比Y Z多,半径大,再根据同周期原子半径依次减小规律,推出半径大小顺序:X>W>Y>Z,故A错误;
B.同周期非金属性依次增强,故氢化物稳定性依次增强,热稳定性:H2Y<HZ,故B错误;
C.根据“阴上阳下,径小序大”规律:Y2->W2+,故C错误;
D.同周期元素金属性依次减弱,最高价氧化物对应水化物的碱性依次减弱,碱性:XOH>W(OH)2 ,故D正确.
故选D.
点评:本题考查了元素周期表和元素周期律,为高频考点,侧重于学生的分析能力的考查,题目难度不大,微粒半径大小比较、元素金属性、非金属性强弱判断是高考的频考点.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
下列物质的性质与氢键无关的是( )
| A、冰的密度比液态水的密度小 |
| B、乙醇能跟水以任意比混溶 |
| C、NH3分子比PH3分子稳定 |
| D、在相同条件下,H2O的沸点比H2S的沸点高 |
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料.下列说法正确的是( )
| A、元素A、B组成的化合物可能是NH3 |
| B、一定条件下,元素C、D的最高价氧化物对应的水化物之间不能发生反应 |
| C、C、D、E的半径:C>D>E |
| D、化合物AE与CE具有相同类型的化学键 |
构造原理揭示的电子排布能级顺序,实质是各能级能量高低,若以E表示某能级的能量,下列能量大小顺序中正确的是( )
| A、E(3s)>E(2s)>E(1s) |
| B、E(3s)>E(3p)>E(3d) |
| C、E(4f)>E(4s)>E(5d) |
| D、E(5s)>E(4s)>E(4f) |
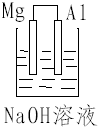 如图所示装置中:
如图所示装置中:
