题目内容
13.下列说法正确的是( )| A. | 乙酸和甲酸甲酯互为同分异构体 | |
| B. | H2和D2互为同素异形体 | |
| C. | CH3CH2OH与HOCH2CH2CH2OH互为同系物 | |
| D. | 35Cl与37Cl为同一种核素 |
分析 A.同分异构体是分子式相同,结构不同的物质互称同分异构体;
B.同素异形体是同种元素形成的不同单质;
C.同系物指分子结构相似,在组成形成1个或若干个CH2原子团物的质;
D.核素是具有一定质子数和中子数的原子.
解答 解:A.乙酸和甲酸甲酯分子式相同,结构不同,互为同分异构体,故A正确;
B.H2和D2是同元素的相同单质,不为同素异形体,故B错误;
C.CH3CH2OH与HOCH2CH2CH2OH,羟基数目不同,结构不相似,不互为同系物,故C错误;
D.35Cl与37Cl为氯元素的不同核素,故D错误.
故选A.
点评 本题考查同素异形体、核素、同分异构体和同系物,题目难度不大,明确相关的定义是解题的关键.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
3.如图是元素周期表前四周期的一部分,关于元素X、Y、Z的叙述错误的是( )
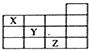

| A. | X的气态氢化物与Y的最高价氧化物的水化物能反应生成盐 | |
| B. | 等物质的量浓度的X、Y、Z的气态氢化物的水溶液的pH:X>Y>Z | |
| C. | Z的单质常温下是液体,可与铁粉反应 | |
| D. | Z的原子序数比Y大9 |
4.氨是一种重要的化工产品,是氮肥工业、有机合成工业以及制造硝酸、铵盐和纯碱等的原料.
(1)以氨为燃料,氧气为氧化剂可以设计制造氨燃料电池,因产物无污染,在很多领域得到广泛应用.若电极材料均为惰性电极,KOH溶液作电解质溶液,则该电池负极电极反应式为2NH3-6e-+6OH-=N2+6H2O;正极分压式为O2+4e-+2H2O=4OH-.
(2)下列措施可以加快合成氨反应速率的是ACDE.
A.通过缩小容器的容积增大压强
B.及时将氨液化分离出去
C.适当升温
D.添加合适的催化剂
E.恒温恒容时,再充入一定体积的氮气
(3)某化学研究性学习小组模拟工业合成氨的反应.在容积固定为2L的密闭容器内充入1mol N2和3mol H2,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下:
则从反应开始到25min时,①以N2表示的平均反应速率为0.01mol/(L.min);②H2的平衡转化率为50%;
(4)以CO2与NH3为原料合成尿素[化学式为CO(NH2)2]的主要反应如下,已知:
①2NH3(g)+CO2(g)═NH2CO2NH4(s);△H=-159.47kJ•mol-1
②NH2CO2NH4(s)═CO(NH2)2(s)+H2O(g);△H=+116kJ•mol-1
③H2O(l)═H2O(g);△H=+44kJ•mol-1
写出CO2与NH3合成尿素和液态水的热化学反应方程式CO2(g)+2NH3(g)=CO(NH2)2(S)+H2O(1)△H=-87.47kJ/mol.
(1)以氨为燃料,氧气为氧化剂可以设计制造氨燃料电池,因产物无污染,在很多领域得到广泛应用.若电极材料均为惰性电极,KOH溶液作电解质溶液,则该电池负极电极反应式为2NH3-6e-+6OH-=N2+6H2O;正极分压式为O2+4e-+2H2O=4OH-.
(2)下列措施可以加快合成氨反应速率的是ACDE.
A.通过缩小容器的容积增大压强
B.及时将氨液化分离出去
C.适当升温
D.添加合适的催化剂
E.恒温恒容时,再充入一定体积的氮气
(3)某化学研究性学习小组模拟工业合成氨的反应.在容积固定为2L的密闭容器内充入1mol N2和3mol H2,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
(4)以CO2与NH3为原料合成尿素[化学式为CO(NH2)2]的主要反应如下,已知:
①2NH3(g)+CO2(g)═NH2CO2NH4(s);△H=-159.47kJ•mol-1
②NH2CO2NH4(s)═CO(NH2)2(s)+H2O(g);△H=+116kJ•mol-1
③H2O(l)═H2O(g);△H=+44kJ•mol-1
写出CO2与NH3合成尿素和液态水的热化学反应方程式CO2(g)+2NH3(g)=CO(NH2)2(S)+H2O(1)△H=-87.47kJ/mol.
1.下列各组物质中,一定互为同系物的是( )
| A. | 乙烷和己烷 | B. | CH3COOH、C3H6O2 | C. |  和 和 | D. | C2H4、C4H8 |
18.下列化学用语不正确的是( )
| A. | CO2分子的电子式为: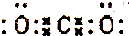 | |
| B. | 质子数为x,中子数为y的氧元素的核素符号为${\;}_{x}^{x+y}$O | |
| C. | Cl-的离子结构示意图为 | |
| D. | HClO的结构式为H-Cl-O |
5.下列关于元素周期表的叙述中正确的是( )
| A. | 元素周期表共有18个族 | |
| B. | 含有元素种类最多的族是第ⅠA 族 | |
| C. | 含有元素种类最多的周期是第六周期 | |
| D. | 第五周期有14种金属元素 |
3.短周期主族元素X、Y、Z、W原子序数依次增大,X原子最外层电子数是次外层的3倍,Z原子最外层只有1个电子,W的最低负价为-3.下列叙述正确的是( )
| A. | X与W的最高正价之和为11 | |
| B. | Y的氢化物的稳定性比W的强 | |
| C. | 原子半径由大到小的顺序为W、Z、Y、X | |
| D. | Y分别与X、Z形成的化合物中化学键类型相同 |