题目内容
8.下列叙述中,不正确的是( )| A. | 钢铁在干燥的环境中不易腐蚀 | |
| B. | 原电池工作时,电解质溶液中的阳离子移向正极 | |
| C. | 用铝质铆钉铆接铁板,铆接处的铁板更易被腐蚀 | |
| D. | 集中回收处理废旧电池的主要目的是防止电池中的重金属离子污染土壤和水源 |
分析 A、钢铁在潮湿的、有氧的环境下更易腐蚀;
B、原电池中阳离子向正极移动;
C、Al比Fe活泼,保护了Fe;
D、电池中含有的汞、铜等重金属对土壤和水源具有污染性;
解答 解:A、钢铁在潮湿的、有氧的环境下更易腐蚀,则钢铁在干燥的环境中不易腐蚀,故A正确;
B、原电池中阳离子向正极移动,电解质溶液中的阳离子移向正极,故B正确;
C、Al比Fe活泼,保护了Fe,故C错误;
D、电池中含有的汞、铜等重金属对土壤和水源具有污染性,主要目的是防止污染地下水和土壤,故D正确;
故选C.
点评 本题考查了金属的腐蚀与防护,作原电池负极、电解池阳极的金属易被腐蚀,难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
3.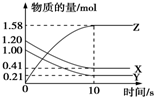 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( )
 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( )| A. | 反应开始到10 s,用Z表示的反应速率为0.158 mol•L-1•s-1 | |
| B. | 反应开始到10 s时,平均反应速率:v(X)=v(Y)=0.039 5 mol•L-1•s-1 | |
| C. | 10 s后,该反应停止进行 | |
| D. | 反应的化学方程式为2X(g)+Y(g)?2Z(g) |
4.下列说法正确的是( )
| A. | 蛋白质与氨基酸一样也是两性分子,既能与酸反应,又能与碱反应 | |
| B. | 豆浆中富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 | |
| C. | 浓Na2SO4溶液能使蛋白质溶液中的蛋白质析出,加水后析出的蛋白质又溶解,但已失去生理活性 | |
| D. | 核酸是由C、H、0、P、N等元素组成的小分子有机物 |
16.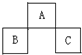 A、B、C均为周期表中的短周期的元素,它们在周期表的位置如下图.已知B、C两元素在周期表中族数之和是A元素族数的2倍;B、C元素的原子序数之和是A 元素的原子序数的4倍,则A、B、C所在的一组是 ( )
A、B、C均为周期表中的短周期的元素,它们在周期表的位置如下图.已知B、C两元素在周期表中族数之和是A元素族数的2倍;B、C元素的原子序数之和是A 元素的原子序数的4倍,则A、B、C所在的一组是 ( )
 A、B、C均为周期表中的短周期的元素,它们在周期表的位置如下图.已知B、C两元素在周期表中族数之和是A元素族数的2倍;B、C元素的原子序数之和是A 元素的原子序数的4倍,则A、B、C所在的一组是 ( )
A、B、C均为周期表中的短周期的元素,它们在周期表的位置如下图.已知B、C两元素在周期表中族数之和是A元素族数的2倍;B、C元素的原子序数之和是A 元素的原子序数的4倍,则A、B、C所在的一组是 ( )| A. | Be、Na、Al | B. | P、O、Cl | C. | O、P、Cl | D. | C、Al、P |
3.下列有关金属的工业制法中,不正确的是( )
| A. | 制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液 | |
| B. | 制镁:用海水为原料,经一系列过程制得氯化镁固体,电解熔融的氯化镁得镁 | |
| C. | 制铁:以铁矿石为原料,CO还原得铁 | |
| D. | 制铝:从铝土矿中获得氧化铝,提纯后电解熔融的氧化铝得到铝 |
13.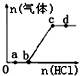 向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
 向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )| A. | a点对应的溶液中:Na+、Ca2+、SO42-、NO3- | |
| B. | b点对应的溶液中:K+、Na+、OH-、Cl- | |
| C. | c点对应的溶液中:Na+、Ca2+、NO3-、Cl- | |
| D. | d点对应的溶液中:Cl-、NO3-、Fe2+、Na+ |
17.“绿色化学”对化学反应提出了“原子经济性”(原子节约)的新概念及要求,理想原子经济性反应是原料分子中的原子全部转化成所需要的产物,不产生副产物,实现零排放.下列反应类型一定符合这一要求的是( )
①取代反应 ②加成反应 ③消去反应 ④水解反应 ⑤加聚反应 ⑥酯化反应.
①取代反应 ②加成反应 ③消去反应 ④水解反应 ⑤加聚反应 ⑥酯化反应.
| A. | ①④ | B. | ②③ | C. | ⑤⑥ | D. | ②⑤ |
18.下列图象所表示的化学知识中,不正确的是( )
| A. | 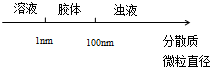 分散系的分类 | B. | 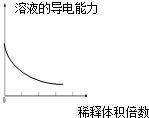 稀释浓氢氧化钠溶液的过程 | ||
| C. | 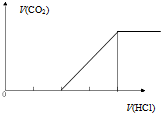 向碳酸钠溶液中逐滴滴加盐酸 | D. |  向偏铝酸钠溶液中逐滴滴加盐酸 |
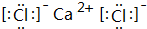 .
.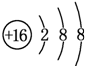 ;D与E能形成一种结构类似于CO2的三原子分子,且每个原子均达到了8电子的稳定结构,该分子的结构式为S=C=S.
;D与E能形成一种结构类似于CO2的三原子分子,且每个原子均达到了8电子的稳定结构,该分子的结构式为S=C=S.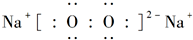 (填电子式),其化学键类型为离子键、非极性共价键(填“离子键”、“非极性共价键”、“极性共价键”中的一种或多种).
(填电子式),其化学键类型为离子键、非极性共价键(填“离子键”、“非极性共价键”、“极性共价键”中的一种或多种).