题目内容
大功率Al一H2O2动力电池原理如图所示,下列说法不正确的是( )


| A、电池组成中Al电极是负极 |
| B、OH-从碳纤维电极透过离子交换膜移向Al电极 |
| C、碳纤维电极的电极反应是H2O2+2e-+2H+=2H2O |
| D、该电池反应的离子方程式是:2Al+3H2O2+2OH-=2AlO2-+4H2O |
考点:化学电源新型电池
专题:电化学专题
分析:该原电池中,Al易失电子作负极、C作正极,负极反应式为Al-3e-+4OH-=2H2O+AlO2-,正极反应式为H202+2e-=2OH-,得失电子相等条件下正负极电极反应式相加得到电池反应式2Al+3H2O2+2OH-=2AlO2-+4H2O,放电时,电解质溶液中阴离子向负极移动,据此分析解答.
解答:
解:该原电池中,Al易失电子作负极、C作正极,负极反应式为Al-3e-+4OH-=2H2O+AlO2-,正极反应式为H202+2e-=2OH-,得失电子相等条件下正负极电极反应式相加得到电池反应式2Al+3H2O2+2OH-=2AlO2-+4H2O,
A.该原电池中Al易失电子作负极,故A正确;
B.Al是负极,放电时电解质中阴离子向负极移动,所以OH-从碳纤维电极透过离子交换膜移向Al电极,故B正确;
C.正极反应式为H202+2e-=2OH-,故C错误;
D.得失电子相等条件下正负极电极反应式相加得到电池反应式2Al+3H2O2+2OH-=2AlO2-+4H2O,故D正确;
故选C.
A.该原电池中Al易失电子作负极,故A正确;
B.Al是负极,放电时电解质中阴离子向负极移动,所以OH-从碳纤维电极透过离子交换膜移向Al电极,故B正确;
C.正极反应式为H202+2e-=2OH-,故C错误;
D.得失电子相等条件下正负极电极反应式相加得到电池反应式2Al+3H2O2+2OH-=2AlO2-+4H2O,故D正确;
故选C.
点评:本题考查化学电源新型电池,明确原电池原理即可解答,难点是电极及电池反应式的书写,要结合电解质溶液书写,为学习难点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
可逆反应L(s)+G(g)?2R(g),由图分析y所表示的量以及反应的能量变化为(图中压强P1>P2>P3( )
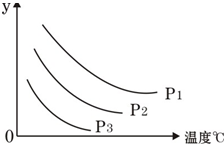

| A、G的体积分数,正反应为吸热反应 |
| B、R的体积分数,正反应为吸热反应 |
| C、G的转化率,正反应为放热反应 |
| D、R的分解率,正反应为放热反应 |
氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于区域3的是( )
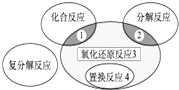

A、2H2+O2
| ||||
| B、Zn+H2SO4=ZnSO4+H2↑ | ||||
C、CuO+CO
| ||||
D、2NaHCO3
|
铅蓄电池是广泛应用于汽车、柴油机车等的启动电源.下列有关铅蓄电池的说法不正确的是( )
| A、铅蓄电池在充电时,原来负极发生的反应是:Pb+SO42--2e-?PbSO4 |
| B、铅蓄电池的电解质溶液是硫酸溶液,在放电过程中,它的浓度逐渐降低 |
| C、铅蓄电池在放电时,电子从Pb通过导线流向PbO2 |
| D、铅蓄电池放电时为原电池,充电时为电解池 |
下列化学用语或模型图示正确的是( )
A、核内有8个中子的碳原子:
| ||
B、Mg2+的结构示意图: | ||
C、Na2O2的电子式: | ||
D、聚丙烯的结构简式: |
逻辑推理是化学学习中常用的一种思维方法.以下推理中正确的是( )
| A、化合物都是由不同元素组成的,故不同元素组成的物质一定是化合物 |
| B、金属镁在金属活动性顺序表中位于氢之前,故其与硝酸反应一定放出氢气 |
| C、中和反应都有盐和水生成,故有盐和水生成的反应都属于中和反应 |
| D、氧化物中都含有氧元素,故含有氧元素的化合物可能是氧化物 |