题目内容
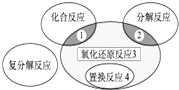
氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于区域3的是( )

A、2H2+O2
| ||||
| B、Zn+H2SO4=ZnSO4+H2↑ | ||||
C、CuO+CO
| ||||
D、2NaHCO3
|
考点:氧化还原反应
专题:氧化还原反应专题
分析:由图可知,区域3所表示的反应是氧化还原反应,但不是置换反应,不是化合反应,不是分解反应,有元素化合价变化的反应为氧化还原反应,以此来解答.
解答:
解:A、反应是氧化还原反应,也是化合反应,不属于区域3,故A错误;
B、该反应是氧化还原反应,但又是置换反应,不属于区域3,故B错误;
C、反应是氧化还原反应,不是置换反应,不是化合反应,不是分解反应,属于区域3,故C正确;
D、反应不是氧化还原反应,是分解反应,不属于区域3,故D错误.
故选C.
B、该反应是氧化还原反应,但又是置换反应,不属于区域3,故B错误;
C、反应是氧化还原反应,不是置换反应,不是化合反应,不是分解反应,属于区域3,故C正确;
D、反应不是氧化还原反应,是分解反应,不属于区域3,故D错误.
故选C.
点评:本题考查氧化还原反应及四种基本反应类型,明确反应的分类及反应中元素的化合价变化是解答本题的关键,题目难度不大.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
2009年10月1日,在天安门广场举行了隆重的国庆阅兵仪式,展现了我国强大的综合国力,其中坦克的展示无疑是一个巨大的亮点.坦克的制造材料主要是各种金属的合金,钢铁便是其中十分重要的一种.下列关于铁的说法中,正确的是( )
| A、铁元素属于过渡元素,其原子序数为26 |
| B、单质铁与浓硫酸在常温下不反应 |
| C、铁单质只具有还原性,其阳离子只具有氧化性 |
| D、与相同浓度的盐酸反应生成氢气的速率,纯铁比生铁的快 |
对下列过程中发生反应的叙述正确的是( )
| A、从铝土矿中分离出氧化铝的过程中不涉及氧化还原反应 |
| B、纯净的二氧化硅有优良的光学性能,可制成光电池和光导纤维 |
| C、海水中含有大量的钠元素,只需经过物理变化就可以得到钠单质 |
| D、Na+、Mg2+、Al3+得电子能力很弱,故常用电解熔融氧化物的方法来制备其单质 |
Mg-AgCl电池是一种用海水激活的一次电池,在军事上用作电动鱼雷的电源.电池的总反应可表示为:Mg+2AgCl═MgCl2+2Ag下列关于该电池的说法错误的是( )
| A、该电池工作时,正极反应为:2AgCl+2e-═2C1-+2Ag |
| B、该电池的负极材料可以用金属铝代替 |
| C、有24g Mg被氧化时,可还原得到108gAg |
| D、装备该电池的鱼雷在水中行进时,海水作为电解质溶液 |
大功率Al一H2O2动力电池原理如图所示,下列说法不正确的是( )


| A、电池组成中Al电极是负极 |
| B、OH-从碳纤维电极透过离子交换膜移向Al电极 |
| C、碳纤维电极的电极反应是H2O2+2e-+2H+=2H2O |
| D、该电池反应的离子方程式是:2Al+3H2O2+2OH-=2AlO2-+4H2O |
在下列各溶液中,一定能大量共存的离子组是( )
| A、强碱性溶液中:K+、Mg2+、Cl-、SO42- |
| B、水电离出来的c(H+)=10-13mol/L的溶液 K+、HCO3-、Br-、Ba2+ |
| C、所含溶质为Na2SO4的溶液 K+、CO32-、NO3-、Al3+ |
| D、室温下,pH=1的溶液中:Na+、Fe3+、NO3-、SO42- |
下列有关0.1mol?L-1 NaOH 溶液的叙述正确的是( )
| A、0.1L该溶液中含有NaOH 4.0g |
| B、从1L该溶液中取出100mL,所取出的NaOH溶液的浓度为0.01 mol?L-1 |
| C、100 mL该溶液中含有OH-0.01mol |
| D、在1 L水中溶解4g NaOH即可配制得0.1 mol?L-1NaOH溶液 |