题目内容
下列说法正确的是( )
| A、0.5molH2O2中含有6.02×1023个质子 |
| B、1molC5H12分子中含有17×6.02×1023个共用电子对 |
| C、质量均为16g 的O2和O3中都含有6.02×1023个原子 |
| D、标准状况下,11.2LHCl中含6×6.02×1023个离子 |
考点:阿伏加德罗常数
专题:
分析:A、1molH2O2中含18mol质子;
B、根据一个C5H12中含有16个共用电子对;
C、根据O2和O3均由 氧原子构成来计算;
D、HCl是共价化合物,无离子.
B、根据一个C5H12中含有16个共用电子对;
C、根据O2和O3均由 氧原子构成来计算;
D、HCl是共价化合物,无离子.
解答:
解:A、1molH2O2中含18mol质子,故0.5molH2O2中含9mol质子,故A错误;
B、一个C5H12中含有16个共用电子对,所以1molC5H12分子中含有16×6.02×1023个共用电子对,故B错误;
C、16gO2和O3混合气体中氧原子的物质的量n=
=
=1mol,个数为6.02×1023个,故C正确;
D、HCl是共价化合物,无离子,故D错误.
故选C.
B、一个C5H12中含有16个共用电子对,所以1molC5H12分子中含有16×6.02×1023个共用电子对,故B错误;
C、16gO2和O3混合气体中氧原子的物质的量n=
| m |
| M |
| 16g |
| 16g/mol |
D、HCl是共价化合物,无离子,故D错误.
故选C.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大

练习册系列答案
相关题目
我们食用的大豆,最终补充给人体的主要成分是( )
| A、氨基酸 | B、蛋白质 |
| C、多肽 | D、糖类 |
在一定体积的18mol/L的浓硫酸中加入过量铜片并加热,被还原的硫酸为0.9mol,则浓H2SO4的实际体积( )
| A、等于50mL |
| B、大于50mL |
| C、等于100mL |
| D、大于100mL |
下列有关实验操作的叙述不正确的是( )
| A、用干燥、洁净的玻璃棒醮取待测液滴在 pH试纸(置于表面皿内)上测溶液的pH |
| B、烧瓶、锥形瓶、烧杯加热时都要垫石棉网 |
| C、制备Fe(OH)3胶体时,应往沸水中加饱和FeC13溶液,并继续加热至溶液呈现红褐色为止 |
| D、已知I3-?I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 |
下列物质中属于电解质的是( )
①氢氧化钠 ②硫酸钡 ③铜 ④蔗糖 ⑤二氧化硫 ⑥浓盐酸.
①氢氧化钠 ②硫酸钡 ③铜 ④蔗糖 ⑤二氧化硫 ⑥浓盐酸.
| A、①② | B、①②⑤ |
| C、④⑤ | D、①②⑥ |
制取新型水处理剂CO2的化学方程式为:2KClO3+H2C2O4+H2SO4
2ClO2+K2SO4+2CO2+2H2O.下列说法不正确的是( )
| ||
| A、KClO3在反应中得到电子 |
| B、1mol KClO3参加反应有2mol电子转移 |
| C、H2C2O4在反应中被氧化 |
| D、ClO2是还原产物 |
下列化学方程式或离子方程式正确的是( )
| A、乙酸与碳酸钠溶液反应:2H++CO32-=CO2↑+H2O | ||
B、甲醛与足量新制Cu(OH)2浊液反应:HCHO+2Cu(OH)2
| ||
C、实验室用液溴和苯在催化剂作用下制溴苯: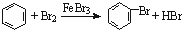 | ||
D、将CO2通入苯酚钠溶液: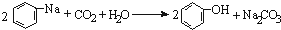 |