题目内容
某同学设计以下实验,证明NaOH溶液能使酚酞试液变红是OH-的性质,其中实验设计不合理的是( )A.取KOH、Ca(OH)2、Ba(OH)2溶液分别与酚酞试液作用,观察溶液颜色
B.取NaOH、NaCl、HCl溶液分别与酚酞试液作用,观察溶液颜色
C.向滴有酚酞的20.0mL0.10mol·L-1 NaOH溶液中,逐滴加入25.0 mL 0.10mol·L-1的盐酸,观察溶液颜色变化
D.向滴有酚酞的25.0 mL0.10mol·L-1盐酸中,逐滴加入20.0mL0.10mol·L-1的NaOH溶液,观察溶液颜色变化
D
【解析】 本题考查实验设计和评价能力。A中阳离子各不相同,但都使酚酞变红,说明是OH造成的,对;B中NaOH变红,但NaCl不变红,说明不是Na+而是OH-引起的,对;C中开始变红,溶液中有Na+和OH-两种,再加HCl到过量,溶液颜色褪去,说明当初是OH-造成的,因为Na+没变;D中NaOH不足,始终不会有颜色变化,所以无法判定。

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案
相关题目
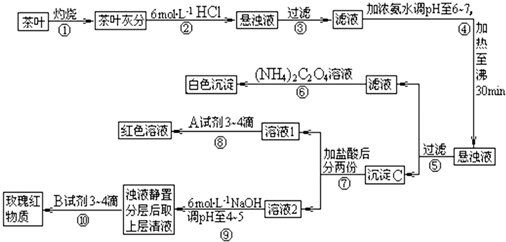
某校化学兴趣小组的同学设计以下实验来定性检验茶叶中含有钙、铁、铝三种金属元素.【已知完全沉淀的pH:Ca(OH)2:pH≥13;Al(OH)3:pH≥5.5;Fe(OH)3:pH≥4.1】
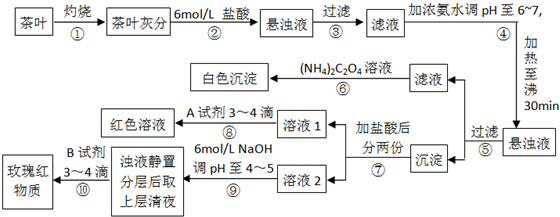
下列说法不正确的是( )

下列说法不正确的是( )
| A、步骤②加入6mol/L盐酸的主要目的是为了将茶叶灰分中的钙、铁、铝难溶性化合物转化为可溶性氯化物 | B、步骤⑤所得滤液中溶质的主要成分为:CaCl2、NH3?H2O | C、步骤⑥可以检出钙元素存在,离子反应方程式为Ca2++C2O42-═CaC2O4↓ | D、步骤⑧中A试剂为KSCN溶液,离子反应方程式为Fe3++3SCN-?Fe(SCN)3 |
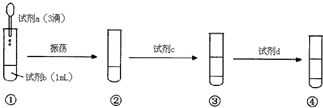 某同学用以下实验用品设计验证碘化钾与氯化铁反应的限度:0.1mol?L-1 KI溶液0.1mol?L-1 FeCl3溶液、CCl4、淀粉溶液、KSCN溶液、试管、胶头滴管等.该同学设计的实验方案如图:根据以上实验方案判断下列说法不正确的是( )
某同学用以下实验用品设计验证碘化钾与氯化铁反应的限度:0.1mol?L-1 KI溶液0.1mol?L-1 FeCl3溶液、CCl4、淀粉溶液、KSCN溶液、试管、胶头滴管等.该同学设计的实验方案如图:根据以上实验方案判断下列说法不正确的是( )| A、试剂a是0.1mol?L-1 KI溶液 | B、试剂d是KSCN溶液 | C、说明该反应已经发生的理由是③的下层呈紫色 | D、说明该反应是有限度的实验现象是④的上层溶液出现血红色 |