题目内容
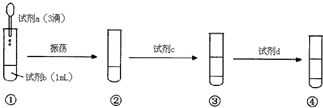 某同学用以下实验用品设计验证碘化钾与氯化铁反应的限度:0.1mol?L-1 KI溶液0.1mol?L-1 FeCl3溶液、CCl4、淀粉溶液、KSCN溶液、试管、胶头滴管等.该同学设计的实验方案如图:根据以上实验方案判断下列说法不正确的是( )
某同学用以下实验用品设计验证碘化钾与氯化铁反应的限度:0.1mol?L-1 KI溶液0.1mol?L-1 FeCl3溶液、CCl4、淀粉溶液、KSCN溶液、试管、胶头滴管等.该同学设计的实验方案如图:根据以上实验方案判断下列说法不正确的是( )| A、试剂a是0.1mol?L-1 KI溶液 | B、试剂d是KSCN溶液 | C、说明该反应已经发生的理由是③的下层呈紫色 | D、说明该反应是有限度的实验现象是④的上层溶液出现血红色 |
分析:A.试剂a是0.1mol?L-1 FeCl3溶液;
B.需KI溶液过量,保证FeCl3溶液充分反应,可以用KSCN溶液(即操作④,试剂d),来检验三价铁是否剩余;
C.四氯化碳密度大于水,在下层,碘单质易溶于四氯化碳,混合液分层,四氯化碳层呈紫红色在下层,有碘生成说明反应已经开始;
D.通过验证有Fe3+残留,说明该反应是有限度,硫氰根离子与铁离子显示血红色;
B.需KI溶液过量,保证FeCl3溶液充分反应,可以用KSCN溶液(即操作④,试剂d),来检验三价铁是否剩余;
C.四氯化碳密度大于水,在下层,碘单质易溶于四氯化碳,混合液分层,四氯化碳层呈紫红色在下层,有碘生成说明反应已经开始;
D.通过验证有Fe3+残留,说明该反应是有限度,硫氰根离子与铁离子显示血红色;
解答:解:A.该实验的目的是验证碘化钾与氯化铁反应的限度,通过验证有Fe3+残留,从而证明化学反应有一定的限度,所以需KI溶液过量,保证FeCl3溶液充分反应,所以试剂a是0.1mol?L-1 FeCl3溶液,故A错误;
B.可以用KSCN溶液(即操作④,试剂d),来检验三价铁是否剩余,如果溶液显红色,说明三价铁剩余,KI溶液和FeCl3溶液反应不彻底,反之则进行彻底,所以试剂d是KSCN溶液,故B正确;
C.滴加试剂CCl4,(即操作③,试剂C)用力振荡一段时间,下层CCl4出现紫红色,说明有碘生成,KI和FeCl3发生反应:2KI+FeCl3=I2+2KCl+FeCl2,故C正确;
D.说明该反应是有限度,通过验证有Fe3+残留,铁离子能够与硫氰根离子反应生成红色的络合物硫氰化铁,据此检验铁离子是否存在,所以实验现象是④的上层溶液出现血红色,说明该反应是有限度,故D正确;
故选A.
B.可以用KSCN溶液(即操作④,试剂d),来检验三价铁是否剩余,如果溶液显红色,说明三价铁剩余,KI溶液和FeCl3溶液反应不彻底,反之则进行彻底,所以试剂d是KSCN溶液,故B正确;
C.滴加试剂CCl4,(即操作③,试剂C)用力振荡一段时间,下层CCl4出现紫红色,说明有碘生成,KI和FeCl3发生反应:2KI+FeCl3=I2+2KCl+FeCl2,故C正确;
D.说明该反应是有限度,通过验证有Fe3+残留,铁离子能够与硫氰根离子反应生成红色的络合物硫氰化铁,据此检验铁离子是否存在,所以实验现象是④的上层溶液出现血红色,说明该反应是有限度,故D正确;
故选A.
点评:本题是一道验证碘化钾与氯化铁反应的限度的题目,要求学生具有分析和解决问题的能力,注意三价铁离子的检验是高频考点,题目难度较大.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
(1)(4分)某同学用质量分数为98%、密度为1.84 g/cm3的浓硫酸,配制184 mL 2 mol/L H2SO4溶液,并进行有关的实验。试回答下列问题:
![]() ①计算所需浓硫酸的体积 ml。
①计算所需浓硫酸的体积 ml。
![]() ②从下列仪器中选出实验所需要的仪器 (填序号)。
②从下列仪器中选出实验所需要的仪器 (填序号)。
![]() A.10 mL量筒 B.20 mL量筒 C.100 mL烧杯 D.250 mL容量瓶 E.托盘天平
A.10 mL量筒 B.20 mL量筒 C.100 mL烧杯 D.250 mL容量瓶 E.托盘天平
![]() F.分液漏斗 G.玻璃棒 I.胶头滴管
F.分液漏斗 G.玻璃棒 I.胶头滴管
![]() (2)(6分)以下厨房用品中都混有杂质(括号内物质),请选择适当的化学试剂进行检测,将其标号填入对应的空格中;并请填写出观察到的现象。
(2)(6分)以下厨房用品中都混有杂质(括号内物质),请选择适当的化学试剂进行检测,将其标号填入对应的空格中;并请填写出观察到的现象。
![]()
| 实验要求 | 化学试剂
| 现 象 |
| 酒精(水) |
| |
| 味精(小苏打) |
| |
| 蔗糖(葡萄糖) |
|
供选试剂:A.新制氢氧化铜悬浊液 B.醋酸 C.碘水 D.无水硫酸铜粉末