题目内容
12.对下列实验指定容器中的水,其解释没有体现水的主要作用的是( )| A | B | C | D | |
| 实验装置 | 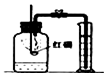 测定空气中氧气含量 | 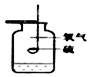 硫在氧气中燃烧 | 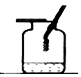 铁丝在氧气中燃烧 | 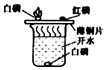 探究燃烧的条件 |
| 解释 | 量筒中水:通过水体积的变化得出O2的体积 | 集气瓶中的水:吸收放出的热量 | 集气瓶中的水:冷却溅落熔融物,防止集气瓶炸裂 | 烧杯中的水:加热铜片;隔绝空气 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.集气瓶中P与氧气反应,则量筒中水进入集气瓶;
B.S燃烧为放热反应;
C.Fe燃烧生成四氧化三铁,高温下易使集气瓶炸裂;
D.探究燃烧的条件,隔绝空气,开水的温度高.
解答 解:A.集气瓶中P与氧气反应,则量筒中水进入集气瓶,则通过水体积的变化得出O2的体积,故A正确;
B.S燃烧为放热反应,不需要集气瓶中的水吸热,故B错误;
C.Fe燃烧生成四氧化三铁,高温下易使集气瓶炸裂,则集气瓶中的水可冷却溅落熔融物,防止集气瓶炸裂,故C正确;
D.探究燃烧的条件,隔绝空气,开水的温度高,则烧杯中的水可加热铜片、隔绝空气,故D正确;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握图中实验装置的作用、实验原理为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识与实验的结合,题目难度不大.

练习册系列答案
相关题目
2.配制一定物质的量浓度的稀硫酸溶液时,实验结果偏高的是( )
| A. | 定容时仰视液面 | |
| B. | 溶解后立即转移到容量瓶中 | |
| C. | 未洗涤烧杯和玻璃棒 | |
| D. | 溶液配好摇匀后,发现液面低于刻度线,又加水至液面与刻度线相切 |
7.下列关于有机物的说法正确的是( )
| A. | 乙醇、乙烷和乙酸都可以与钠反应生成氢气 | |
| B. | 70%-75%(体积分数)的乙醇溶液常用于医疗消毒 | |
| C. | 苯和乙烯都可以使溴的四氯化碳溶液褪色 | |
| D. | 石油分馏可获得乙酸、苯及甲苯 |
17.如表是某食品包装袋上的说明,从表中的配料中分别选出一种物质填在相应的横线上.
其中属于着色剂的有柠檬黄、日落黄;属于调味剂的有蔗糖、柠檬酸、甜蜜素、菠萝香精;属于防腐剂的有山梨酸钾;富含维生素的有浓缩菠萝汁、维生素C.
蛋白质的性质在生活中有许多实际应用.请在下表“性质”一栏中用“盐析”、“变性”或“颜色反应”表述的蛋白质性质填空.
| 品名 | 浓缩菠萝汁 |
| 配料 | 水、浓缩菠萝汁、蔗糖、柠檬酸、甜蜜素、维生素C、菠萝香精、 柠檬黄、日落黄、山梨酸钾等 |
| 果汁含量 | ≥80%生产日期标于包装袋封口上 |
蛋白质的性质在生活中有许多实际应用.请在下表“性质”一栏中用“盐析”、“变性”或“颜色反应”表述的蛋白质性质填空.
| 实例 | 性质 |
| 紫外线消毒 | 变性 |
| 蛋白质遇浓硝酸变黄 | |
| 误食了重金属离子,可以立即喝大量的牛奶来缓解 毒性 | |
| 鸡蛋清溶液中加入少量饱和的硫酸铵溶液出现沉淀 | |
| 常用酒精清洗伤口 | |
| 蒸煮鸡蛋食用 |
1.可以用氯气灌洞的方法来消灭田鼠,这是利用了氯气的哪些性质( )
①密度比空气的大 ②易液化 ③能溶于水 ④有毒.
①密度比空气的大 ②易液化 ③能溶于水 ④有毒.
| A. | ①④ | B. | ①② | C. | ③④ | D. | ①③④ |
8.碳及其化合物有广泛的用途.
(1)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)═CO(g)+H2(g)△H>0,以上反应达到平衡后,在体积不变的条件下,以下措施有利于提高H2O(g)的平衡转化率的是AD.
A.升高温度 B.增加碳的用量 C.加入催化剂 D.用CO吸收剂除去CO
(2)将一定量的CO(g)和H2O(g)分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:
CO(g)+H2O(g)═CO2(g)+H2(g),得到如下数据:
通过计算求出该反应的平衡常数(计算结果保留两位有效数字).
(3)把水煤气中的混合气体经过处理后获得的较纯H2用于工业合成氨.已知:
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1
2N2(g)+6H2O(l)═4NH3(g)+3O2(g)△H=+1530.0kJ/mol
①氢气的燃烧热△H=-285.8kJ/mol.
(1)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)═CO(g)+H2(g)△H>0,以上反应达到平衡后,在体积不变的条件下,以下措施有利于提高H2O(g)的平衡转化率的是AD.
A.升高温度 B.增加碳的用量 C.加入催化剂 D.用CO吸收剂除去CO
(2)将一定量的CO(g)和H2O(g)分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:
CO(g)+H2O(g)═CO2(g)+H2(g),得到如下数据:
| 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | ||
| H2O | CO | H2 | CO | ||
| 900 | 1.0 | 2.0 | 0.4 | 1.6 | 3.0 |
(3)把水煤气中的混合气体经过处理后获得的较纯H2用于工业合成氨.已知:
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1
2N2(g)+6H2O(l)═4NH3(g)+3O2(g)△H=+1530.0kJ/mol
①氢气的燃烧热△H=-285.8kJ/mol.
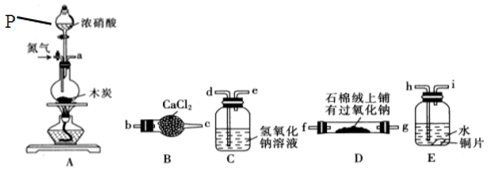
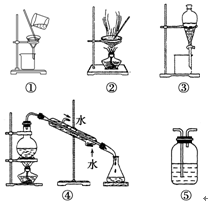
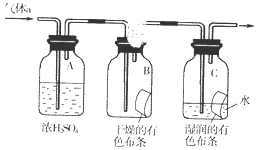 氯气是一种化学性质活泼的非金属单质,工业上可用氯气制取漂白粉、有机溶剂等.
氯气是一种化学性质活泼的非金属单质,工业上可用氯气制取漂白粉、有机溶剂等.