题目内容
7.下列关于有机物的说法正确的是( )| A. | 乙醇、乙烷和乙酸都可以与钠反应生成氢气 | |
| B. | 70%-75%(体积分数)的乙醇溶液常用于医疗消毒 | |
| C. | 苯和乙烯都可以使溴的四氯化碳溶液褪色 | |
| D. | 石油分馏可获得乙酸、苯及甲苯 |
分析 A.乙烷与Na不反应;
B.乙醇可使蛋白质发生变性;
C.苯与溴的四氯化碳溶液不反应;
D.石油为烃类混合物,分馏为物理变化.
解答 解:A.乙烷与Na不反应,而乙醇、乙酸与Na反应生成氢气,故A错误;
B.乙醇可使蛋白质发生变性,则70%-75%(体积分数)的乙醇溶液常用于医疗消毒,故B正确;
C.苯与溴的四氯化碳溶液不反应,而乙烯可以使溴的四氯化碳溶液褪色,发生加成反应,故C错误;
D.石油为烃类混合物,分馏为物理变化,不能分馏得到乙酸,故D错误;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机物的组成及有机反应为解答的关键,侧重分析与应用能力的考查,注意石油分馏产品,题目难度不大.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
17.下列各项实验中,所测得的数据不能满足于测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是( )
| A. | 取ag混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,碱石灰增重bg | |
| B. | 取ag混合物与足量稀盐酸充分反应后,加热蒸干溶液,得bg固体 | |
| C. | 取ag混合物充分加热,得到bg固体 | |
| D. | 取ag混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得bg固体 |
18.下列叙述正确的是( )
| A. | 常温下c(H+)为0.01 mol/L的盐酸由H2O电离出的c(H+)=1.0×10-2mol•L-1 | |
| B. | 室温下,对于0.10 mol•L-1的氨水,加水稀释后,溶液中c(NH4+)•c(OH-)变大 | |
| C. | 有关反应:(tBuNO)2??2(tBuNO),压强越大,反应物的转化率越大 | |
| D. | 反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行,则该反应的△H<0 |
15.固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体的最外电子层结构,则下列有关说法不正确的是( )
| A. | 它与水反应的离子方程式为NH4++H-+H2O=NH3•H2O+H2↑ | |
| B. | NH5中既有共价键又有离子键 | |
| C. | NH5的电子式为 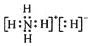 | |
| D. | 1 mol NH5中含有5 NA个N-H键(NA表示阿伏加德罗常数) |
2.下列说法正确的是( )
| A. | 氢化物的沸点:H2O>PH3>NH3 | |
| B. | 第三周期元素(除惰性元素),随着原子序数的递增,元素的最高化合价逐渐升高 | |
| C. | 同主族元素从上到下,非金属性逐渐增强,金属性逐减弱 | |
| D. | P的非金属性强于Si,H2SiO3的酸性强于H3PO4 |
12.对下列实验指定容器中的水,其解释没有体现水的主要作用的是( )
| A | B | C | D | |
| 实验装置 | 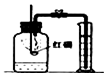 测定空气中氧气含量 | 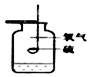 硫在氧气中燃烧 | 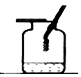 铁丝在氧气中燃烧 | 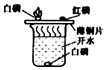 探究燃烧的条件 |
| 解释 | 量筒中水:通过水体积的变化得出O2的体积 | 集气瓶中的水:吸收放出的热量 | 集气瓶中的水:冷却溅落熔融物,防止集气瓶炸裂 | 烧杯中的水:加热铜片;隔绝空气 |
| A. | A | B. | B | C. | C | D. | D |
16.欲配制100mL 1.0mol/LNa2CO3溶液,正确的方法是( )
| A. | 称量10.6 g Na2CO3溶于100 mL水中 | |
| B. | 称量10.6 g Na2CO3•10H2O溶于少量水中,再用水稀释至100 mL | |
| C. | 量取20 mL 5.0 mol/L Na2CO3溶液用水稀释至100 mL | |
| D. | 配制80 mL 1.0 mol/L Na2CO3溶液,则只需要称量8.5 g Na2CO3 |
3.如图所示可逆反应:mA(g)+nB(g)?xC(g),△H=Q kJ/mol,在不同温度、压强下反应物A的转化率的变化情况.下列对于反应的热效应Q和反应方程式A、B、C的化学计量数的判断中,正确的是( )
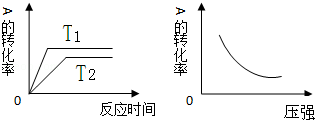

| A. | Q<0,m+n<x | B. | Q<0,m+n>x | C. | Q>0,m+n<x | D. | Q>0,m+n>x |